
| A. | 干馏 | B. | 常压分馏 | C. | 裂解 | D. | 催化重整 |
科目:高中化学 来源: 题型:选择题
 X、Y、Z、W均为短周期元素,在周期表中位置如图所示.Y原子的最外层电于数是内层
X、Y、Z、W均为短周期元素,在周期表中位置如图所示.Y原子的最外层电于数是内层| A. | 气态氢化物的稳定性:Y>Z | |
| B. | 最高价氧化物物对应水化物酸性:Z>W | |
| C. | X的气态氢化物与Y、Z、W的气态氢化物都可以反应 | |
| D. | 气态氢化物的沸点,Y最高 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
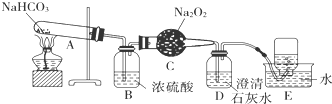
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
| 容器 编号 | 起始时各物质物质的量/mol | 达到平衡的时间/min | 达平衡时体系能量的变化/kJ | |||
| CO | H2O | CO2 | H2 | |||
| ① | 1 | 4 | 0 | 0 | t1 | 放出热量:32.8 kJ |
| ② | 2 | 8 | 0 | 0 | t2 | 放出热量:Q |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | X2+2Y2?2XY2 | B. | 2X2+Y2?2X2Y | C. | X2+3Y2?2XY3 | D. | 3X2+Y2?2X3Y |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 容器编号 | 起始时各物质物质的量(mol) | 达平衡时体系能量的变化 | ||
| X2 | Y2 | XY3 | ||
| ① | 1 | 3 | 0 | 放热 46.3kJ |
| ② | 0.6 | 1.8 | 0.8 | Q (Q>0) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CO2、SO2、NO2都能和碱溶液发生反应,因此它们都属于酸性氧化物 | |
| B. | Na2O2晶体中既含有离子键又含有共价键 | |
| C. | Na2O、Fe2O3、Al2O3属于碱性氧化物 | |
| D. | SiO2不能与水反应生成硅酸,所以SiO2不是酸性氧化物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CO2(SO2):饱和碳酸氢钠溶液 | B. | N2(O2):灼热的铜网 | ||
| C. | Al2O3(SiO2):NaOH溶液 | D. | Na2CO3固体(NaHCO3):加热 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

 .
.
 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com