
实验室制取氧气的反应为2KMnO4 == K2MnO4+MnO2 + 3O2 ↑,反应后从剩余物中回收二氧化锰的操作顺序正确的是
A.溶解、过滤、洗涤、干燥 B.溶解、过滤、蒸发、洗涤
C.溶解、蒸发、洗涤、过滤 D.溶解、洗涤、过滤、加热
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
H2SO3是二元弱酸,NaHSO3溶液呈酸性。在0.1 mol·L-1 NaHSO3溶液
中,下列关系正确的是( )
A.c(HSO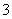 )>c(SO
)>c(SO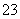 )>c(H2SO3)
)>c(H2SO3)
B.c(Na+)=c(HSO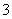 )+2c(SO
)+2c(SO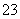 )+c(H2SO3)
)+c(H2SO3)
C.c(Na+)=c(HSO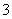 )>c(H+)>c(OH-)
)>c(H+)>c(OH-)
D.c(Na+)+c(H+)=c(HSO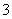 )+c(OH-)+c(SO
)+c(OH-)+c(SO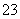 )
)
查看答案和解析>>
科目:高中化学 来源: 题型:
下列离子方程式中,只能表示一个化学反应的是
①Zn+Cu2+ ==Zn2++Cu ②Ag++Cl-== AgCl↓
③Cl2+H2O H++Cl-+HClO ④CO32-+2H+ == CO2↑+H2O
H++Cl-+HClO ④CO32-+2H+ == CO2↑+H2O
A.① B.② C.③ D.④
查看答案和解析>>
科目:高中化学 来源: 题型:
某氮肥硫酸铵中混有硫酸氢铵。为测定该氮肥的含氮量,一化学研究性学习小组设计的实验装置图如下。请回答相关问题:

(1)仪器A的名称为 ,干燥管中碱石灰的作用是 ,广口瓶内四氯化碳的作用是 。
(2)写出硫酸氢铵与过量氢氧化钠溶液反应的离子方程式 。
(3)指导老师指出,用该装置进行实验,即使氢氧化钠足量且实验过程中无氨气外逸,测得的样品含氮量仍将偏低,其原因可能是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
已知:I2+2S2O ===S4O
===S4O +2I-
+2I-
相关物质的溶度积常数见下表:
| 物质 | Cu(OH)2 | Fe(OH)3 | CuCl2 | CuI |
| Ksp | 2.2×10-20 | 2.6×10-39 | 1.7×10-7 | 1.3×10-12 |
(1)某酸性CuCl2溶液中含有少量的FeCl3,为得到纯净的CuCl2·2H2O晶体,加入________,调至pH=4,使溶液中的Fe3+转化为Fe(OH)3沉淀,此时溶液中的c(Fe3+)=________。过滤后,将所得滤液低温蒸发、浓缩结晶,可得到CuCl2·2H2O晶体。
(2)在空气中直接加热CuCl2·2H2O晶体得不到纯的无水CuCl2,原因是____________________________(用化学方程式表示)。由CuCl2·2H2O晶体得到纯的无水CuCl2的合理方法是____________。
(3)某学习小组用“间接碘量法”测定含有CuCl2·2H2O晶体的试样(不含能与I-发生反应的氧化性杂质)的纯度,过程如下:取0.36 g试样溶于水,加入过量KI固体,充分反应,生成白色沉淀。用0.100 0 mol·L-1 Na2S2O3标准溶液滴定,到达滴定终点时,消耗Na2S2O3标准溶液20 .00 mL。
.00 mL。
①可选用_____作滴定指示剂,滴定终点的现象是__________。
②CuCl2溶液与KI反应的离子方程式为___________________。
③该试样中CuCl2·2H2O的质量百分数为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)在0.10 mol·L-1硫酸铜溶液中加入氢氧化钠稀溶液充分搅拌有浅蓝色氢氧化铜沉淀生成,当溶液的pH=8时,c(Cu2+)=________mol·L-1(Ksp[Cu(OH)2]=2.2×10-20)。
(2)若在0.1 mol·L-1硫酸铜溶液中通入过量H2S气体,使Cu2+完全沉淀为CuS,此时溶液中的H+浓度是________mol·L-1。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列图示与对应的叙述相符的是( )

A.图1表示常温下,稀释HA、HB两种酸的稀溶液时,溶液pH随加水量的变化,则NaA溶液的pH小于同浓度的NaB溶液的pH
B.图2表示A、B两物质的溶解度随温度变化情况,将t1 ℃时A、B的饱和溶液分别升温至t2 ℃时,溶质的质量分数 B>A
C.图3表示在其他条件相同时,分别在T1、T2温度下由CO2和H2合成甲醇的物质的量随时间变化情况,则CO2和H2合成甲醇是吸热反应
D.图4表示将1.000 mol·L-1氨水滴入20.00 mL 1.000 mol·L-1盐酸中,溶液pH和温度随加入氨水体积变化曲线
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com