
| A. | B的浓度不再变化 | |
| B. | 混合气体的压强不再变化 | |
| C. | 混合气体的密度不再变化 | |
| D. | 混合气体的平均相对分子质量不再改变 |
分析 当化学反应达到平衡状态时,正逆反应速率相等,各物质的浓度不变,由此衍生的一些物理量也不变,即变量不变说明反应达到平衡状态,注意反应物中A为固体,气体反应物与气体生成物的化学计量数之和相等,反应前后气体质量发生改变.
解答 解:A.当反应达到化学平衡状态时,各物质的浓度不变,是平衡的标志,故A不符合;
B.气体反应物与气体生成物的化学计量数之和相等,反应前后气体压强不变,无论是否达到平衡状态,混合气体总的物质的量都不变,压强始终不变,不能说明反应达到平衡状态,故B符合;
C.在恒温条件下,体积固定的密闭容器中进行可逆反应A(s)+3B(g)?3C(g),反应前后气体质量发生改变,体积不变,ρ=$\frac{m}{V}$不变说明反应达到平衡状态,故C不符合;
D.气体反应物与气体生成物的化学计量数之和相等,气体物质的量不变,A为固体,当反应达到平衡状态时,气体的总质量不变,反应达到平衡状态,故D不符合;
故选B.
点评 本题考查化学平衡状态的判断,题目难度中等,注意把握平衡状态的特征,注意反应物中A为固体,此为解答该题的关键,也是易错点.


 阳光课堂课时优化作业系列答案
阳光课堂课时优化作业系列答案科目:高中化学 来源: 题型:选择题
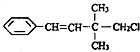 ,关于该有机物的下列叙述中不正确的是( )
,关于该有机物的下列叙述中不正确的是( )| A. | 一定条件下,能发生加聚反应 | |
| B. | 1mol该有机物在一定条件下最多能与4molH2发生反应 | |
| C. | 能使酸性KMnO4溶液、溴水褪色,且原理相同 | |
| D. | 该有机物苯环上的一溴代物有3种 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
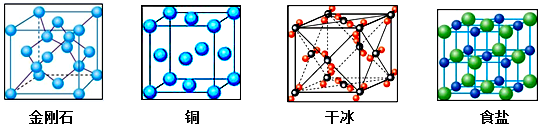
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 使用容量瓶前检查它是否漏水 | |
| B. | 容量瓶用水洗净后,在干燥箱中 干燥 | |
| C. | 配制溶液时,如果试样是固体,把称好的试样用纸条小心倒入容量瓶中,缓慢加水至接近刻度线1~2cm处,用胶头滴管加蒸馏水至刻度线 | |
| D. | 定容后,盖好瓶塞,用食指顶住瓶塞,手握住瓶进颈,左右振荡摇匀 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 4Q1+0.5Q2 | B. | 4Q1+Q2+10Q3 | C. | 4Q1+2Q2 | D. | 4Q1+0.5Q2+9Q3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 25℃时,用浓度为0.1000mol•L-1 的NaOH溶液滴定20mL 浓度均为0.1000mol•L-1的三种酸HX、HY、HZ,滴定曲线如图所示.下列说法正确的是( )
25℃时,用浓度为0.1000mol•L-1 的NaOH溶液滴定20mL 浓度均为0.1000mol•L-1的三种酸HX、HY、HZ,滴定曲线如图所示.下列说法正确的是( )| A. | 在相同温度下,同浓度的三种酸溶液的导电能力顺序:HZ<HY<HX | |
| B. | 根据滴定曲线,可得Ka(HY)≈10-6 | |
| C. | 将上述HX、HY溶液等体积混合后,用NaOH溶液滴定至HX恰好完全反应时:c(X-)>c(Y-)>c(OH-)>c(H+) | |
| D. | HY与HZ混合,达到平衡时:c(H+)═c(Y-)+c(Z-)+c(OH-) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常温常压下,1 L 0.1 mol•L-1 NH4NO3溶液中NH4+、NO3-的数目均为0.1NA | |
| B. | 标准状况下,22.4 L N2和O2的混合气体中含有的原子总数为2NA | |
| C. | 常温常压下,16 g CH4中含有共价键的数目为NA | |
| D. | 16 g CH4与18 g NH4+所含质子数均为10NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 氨是最重要的化工产品之一.
氨是最重要的化工产品之一.| t/℃ | 200 | 300 | 400 |
| K | K1 | K2 | 0.5 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 三种气体质量相等 | B. | 三种气体的物质的量之比为16:2:1 | ||
| C. | 三种气体压强比为16:2:1 | D. | 三种气体体积比为1:8:16 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com