
铬铁矿的主要成分可表示为FeO·Cr2O3,还含有MgO、Al2O3、Fe2O3等杂质,以下是以铬铁矿为原料制备重铬酸钾(K2Cr2O7)的流程图:

已知:①4FeO•Cr2O3+8Na2CO3+7O2  8Na2CrO4+2Fe2O3+8CO2↑;
8Na2CrO4+2Fe2O3+8CO2↑;
②Na2CO3+Al2O3  2NaAlO2+CO2↑;
2NaAlO2+CO2↑;
③Cr2CO72-+H2O 2CrO42-+2H+
2CrO42-+2H+
根据题意回答下列问题:
(1)固体X中主要含有______________(填写化学式);要检测酸化操作中溶液的pH是否等于4.5,应该使用_____________________(填写仪器或试剂名称);
(2)酸化步骤用醋酸调节溶液pH<5,其目的是_____________________;
(3)操作Ⅲ有多步组成,获得K2Cr2O7晶体的操作依次是:加入KCl固体、蒸发浓缩、________、过滤、_______、干燥;
(4)如表是相关物质的溶解度数据,操作III发生反应的化学方程式是:Na2Cr2O7+2KCl→K2Cr2O7+2NaCl,该反应在溶液中能发生的理由是_____________________;
物质 | KCl | NaCl | K2Cr2O7 | Na2Cr2O7 | |
溶解度(g/100g水) | 0℃ | 28 | 35.7 | 4.7 | 163 |
40℃ | 40.1 | 36.4 | 26.3 | 215 | |
80℃ | 51.3 | 38 | 73 | 376 | |
(5)副产品Y主要含氢氧化铝,还含少量镁、铁的难溶化合物及可溶性杂质,精确分析Y中氢氧化铝含量的方法是称取ng样品,加入过量________(填写试剂)、溶解、过滤、再质量分数为________(填写试剂)、…灼烧、冷却、称量,得干燥固体mg.计算祥品中氢氧化铝的________(用含m、n的代数式表示)。
科目:高中化学 来源:2015-2016年陕西西藏民族学院附属中学高二上期末化学卷(解析版) 题型:选择题
下列说法正确的是( )
A.0.1mol/LCH3COOH溶液加水稀释,溶液中c(OH-)增大
B.将NaOH和氨水溶液各稀释一倍,两者的OH-浓度均减少到原来的1/2
C.相同浓度的HCl和CH3COOH,两溶液中c(H+)相同
D.甲溶液的pH是5,乙溶液的pH是4,则甲溶液与乙溶液的中c(H+)之比为10:1
查看答案和解析>>
科目:高中化学 来源:2016届河北省衡水市高三上一轮复习检测二化学试卷(解析版) 题型:选择题
短周期元素X、Y、Z、W在元素周期表中的相对位置如图所示。已知YW的原子序数之和是Z的3倍,下列说法正确的是( )
Y | Z | ||
X | W |
A.原子半径:X<Y<Z
B.气态氢化物的稳定性:X>Z
C.Z、W均可与Mg形成离子化合物
D.最高价氧化物对应水化物的酸性:Y>W
查看答案和解析>>
科目:高中化学 来源:2016届宁夏中卫一中高三上学期期末理综化学试卷(解析版) 题型:选择题
右图表示4-溴环己烯所发生的4个不同的反应,其中,产物中只含有一种官能团的反应是( )
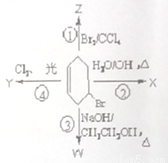
A.①③ B.③④ C.②③ D.①②
查看答案和解析>>
科目:高中化学 来源:2016届陕西省高三上期末化学试卷(解析版) 题型:填空题
某无色废水中可能含有
H+、NH4+、Fe3+、Al3+、Mg2+、Na+、NO3-、CO32-、SO42-中的几种,为分析其成分,分别取废水样品100mL,进行了三组实验,其操作和有关图像如下所示:Ⅰ:
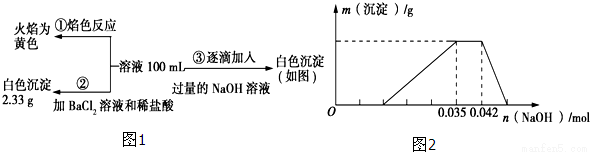
请回答下列问题:
(1)根据上述3组实验可以分析废水中一定不存在的离子有__________;
(2)实验③中所发生反应的离子反应方程式__________;
(3)分析图象,在原溶液中c(NH4+)与c(Al3+)的比值为, NO3-是否存在?__________填(“存在”“不存在”或“不确定”)。
Ⅱ:现有A、B、C、D、E五种可溶性强电解质,它们在水中可电离产生下列离子(各离子不重复)。
阳离子 | H+、Na+、Al3+、Ag+、Ba2+ |
阴离子 | OH-、Cl-、CO32-、NO3-、SO42- |
已知:①A、B两溶液呈碱性;C、D、E溶液呈酸性;
②A溶液与E溶液反应既有气体又有沉淀产生;A溶液与C溶液反应只有气体产生;
③D溶液与另外四种溶液反应都能产生沉淀;C只能与D反应产生沉淀;
④上述沉淀包括难溶物和微溶物.
试回答下列问题:
(1)A溶液呈碱性的原因是__________________(用离子方程式表示);
(2)D是______________溶液,E是______________溶液(均写化学式)。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年甘肃省高二上期末考试化学试卷(解析版) 题型:选择题
煤炭、一氧化碳、氢气都是重要能源,已知:
①C(s)+O2(g)=CO2(g) ΔH1=-393.5 kJ·mol-1
②H2(g)+ 1/2O2(g) =H2O(g) ΔH2=-241.6 kJ·mol-1
③CO(g)+1/2O2(g) =CO2(g) ΔH3=-283.0 kJ·mol-1
④H2O(g)=H2O(l) ΔH4=-44 kJ·mol-1
下列说法合理的是
A.氢气的燃烧热ΔH=-241.6 kJ·mol-1
B.等质量的H2、CO完全燃烧时,CO释放的热量更多
C.煤的气化的热化学方程式为C(s)+H2O(g)=CO(g)+ H2(g) ΔH=-131.1 kJ·mol-1
D.煤炭完全燃烧释放1967.5 kJ热量时转移20 mol电子
查看答案和解析>>
科目:高中化学 来源:2015-2016学年甘肃省高一上期末考试化学试卷(解析版) 题型:选择题
2008年9月25日晚9时10分,我国“神舟七号”载人飞船顺利升入太空。此次火箭的主要燃料是偏二甲肼(用R表示)和四氧化二氮,在火箭发射时,两者剧烈反应产生大量气体并释放出大量的热,该反应的化学方程式为:R + 2N2O4 = 3N2 + 4H2O + 2CO2,下列叙述错误的是 ( )
A.此反应是氧化还原反应 B.反应瞬间产生大量高温气体,推动火箭飞行
C.在反应中N2O4做还原剂 D.R的分子式为C2H8N2
查看答案和解析>>
科目:高中化学 来源:2015-2016学年黑龙江省高一上期末化学试卷(解析版) 题型:选择题
有一块铁的“氧化物”样品,用140 mL 5.0 mol·L-1盐酸恰好将之完全溶解,所得溶液还能吸收0.025 mol Cl2,恰好使其中的Fe2+全部转变为Fe3+,则该样品可能的化学式为( )
A.Fe5O7 B.Fe4O5 C.Fe3O4 D.Fe2O3
查看答案和解析>>
科目:高中化学 来源:2015-2016学年辽宁省高一上学期期末考试化学试卷(解析版) 题型:填空题
金属铜能被氯化铁浓溶液腐蚀,其化学反应是:Cu+2FeCl3=CuCl2+2FeCl2。现将有铜的印刷线路板浸入120mL氯化铁浓溶液中,有9.6g铜被腐蚀掉。取出印刷线路板,向溶液中加入8.4g铁粉,经充分反应,溶液中还存在4.8g不溶解的物质。(设溶液体积不变,且不考虑金属离子水解)。请回答下列问题:
(1)向溶液中加入铁粉后,发生反应的离子反应方程式为 , 。
(2)充分反应后,溶液中存在4.8g不溶物的成分为 。
(3)充分反应后溶液中一定不存在的金属离子为 。
(4)比较Fe2+、Fe3+、Cu2+的氧化性大小: 。
(5)试计算最后溶液中Fe2+离子的物质的量浓度 mol/L
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com