
��գ�
��1��0. 5 mol NH3������������ԭ����Ϊ__________����
��2��1.2g RSO4�к�0.01 mol R2+����RSO4��Ħ��������__________��
��3��0.1 mol��L-1�� Cu(NO3)2��Һ��NO3-�����ʵ���Ũ����__________��
��4��������ˮ�����������²�������ɫ������__________��
��5������100 mL 1 mol/L NaCl��Һ�����ݺ�����ƿ����ҡ�Ⱥ���Һ����ڿ̶��ߣ�����ˮ���̶ȴ���������������Һ���ʵ���Ũ��__________��ѡ�ƫ�ߡ�ƫ�͡���Ӱ�족����
��6��ʵ�����Ʊ�����ʱ���ռ�����������__________����
 ���Ŀ��ּ�����ҵ�����ҵ����������ϵ�д�
���Ŀ��ּ�����ҵ�����ҵ����������ϵ�д� ����ѵ��ϵ�д�
����ѵ��ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2017���㽭ʡ̨���и�����ѧ����ĩ�����������Ի�ѧ�Ծ��������棩 ���ͣ������
Ϊ����֤�����������Ư���ԣ�ʪ�����������Ư���ԣ�ijͬѧ���ʵ������ͼ������B��C��D��E��F�ֱ�ʢ�б���ʳ��ˮ��Ũ���ᡣ�����ɫ������Ũ���ᡢʪ���ɫ������
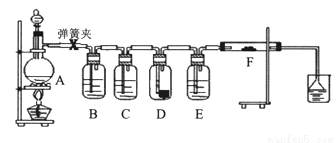
��ش�
��1��E��Ũ���������____________��
��2����F�е�ʪ�������ɾ�����ϸͭ˿�����þƾ��Ƽ��ȣ��ɿ�����������_____________��
��3������װ��A��ȡ2.24L�����������������10mol/LŨ�����������Դ���40mL����ɸý���Ŀ���ԭ����______________��
A.Ũ����Ļӷ� B.�淴Ӧ��������Ũ���½�
C.����ʱ���������� D.MnO2�������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2017�콭��ʡ������ѧ�ڿ�ѧ���Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
����CO2��CH4�������ƺϳ�������Ҫ�ɷ�ΪCO��H2���������й�˵����ȷ����
�� CH4(g) = C(s)+2H2(g) ��H1 = + 75.0 kJ��mol-1
�� CO2(g)+H2(g) = CO(g)+H2O(g) ��H2 = + 41.0 kJ��mol-1
�� CO(g)+H2(g) = C(s)+H2O(g) ��H3 = ��131.0 kJ��mol-1
A. ��Ӧ��Ϊ���ȷ�Ӧ
B. ��Ӧ���л�ѧ��ת��Ϊ����
C. ��Ӧ��ʹ�ô�������H3��С
D. ��ӦCO2(g)+CH4(g)=2CO (g)+2H2 (g)�Ħ�H4 = +247kJ��mol�C1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2017�츣��ʡ�����а�У����2��������ѧ�Ծ��������棩 ���ͣ�ѡ����
���й��ڼס��ҡ���������������װ�õ��й��÷��� ���в��������ǣ�������
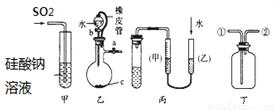
A. ��װ�ã�������֤����ķǽ����Աȹ�ǿ
B. ��װ�ã���Ƥ�ܵ���������ʹˮ˳������
C. ��װ�ã���ͼʾ�ķ����ܼ���װ�õ�������
D. ��װ�ã�����ƿ����װ��ij��Һ���ռ�NO����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2017�츣��ʡ�����а�У����2��������ѧ�Ծ��������棩 ���ͣ�ѡ����
�����ǿ�ѧ�о�����Ҫ�������������ʷ����ȷ����( )
A. ������ɱ�����ˮ�����ռ� B. ͬ�������壺����̿��C60�����ʯ
C. �ǵ���ʣ��Ҵ������Ȼ�̼������ D. ����Ư�ۣ�������Ȫˮ�����ᣬ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016-2017ѧ�꽭��ʡ�����и�һ��ѧ����ĩ���в��Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
��NAΪ�����ӵ�������������������ȷ����
A. 2 mol��L-1 NaCl��Һ�к���Na������Ϊ2NA
B. ��״���£�22.4 L H2O���е�ˮ������ΪNA
C. 71 g�������������۳�ַ�Ӧ��ת�Ƶĵ�����Ϊ3NA
D. ��״���£�16 g O2��O3�Ļ��������ԭ�ӵ����ʵ���Ϊ1mol
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016-2017ѧ�꽭��ʡ�����и�һ��ѧ����ĩ���в��Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
�����Լ��ı��淽���������
A. ������ˮ��������ɫ�Լ�ƿ�� B. ������Na������ú����
C. NaOH��Һ�����ڴ���Ƥ�����Լ�ƿ�� D. ����ᱣ���ڲ����Լ�ƿ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2017��ɽ��ʡ�����и�����ѧ����ĩѧ���϶�����B����ѧ�Ծ��������棩 ���ͣ�ѡ����
��ѧ����С����������������أ������ˮ��Ӧ�ü���㷺������˵��������ˮ���ص��ǣ� ��
A. Na2CO3��NaHCO3���������������ʳ���� B. NaHSO4��Һ������
C. ���ο�������ˮ�� D. TiCl4��Һ�����ɡ������Ƶ�TiO2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016-2017ѧ�꽭��ʡ�ϲ��и�һ��ѧ����ĩ���Ի�ѧ�Ծ��������棩 ���ͣ������
��ҵ�ϴ���������Ҫ�ɷ���Al2O3��������SiO2��Fe2O3�����ʣ�����ȡ����ѡ�����¹������̣�
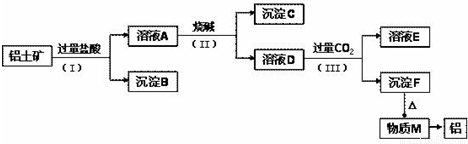
��֪��SiO2������ˮ�Ҳ������ᷴӦ��
��ش��������⣺
��1��ͼ���漰������Һ�������ʵ�鷽����______����������ƣ���
��2�����裨���м�����ռ���ҺӦ����______�����������������������B�ijɷ���______���ѧʽ����ͬ������ҺD�к���Ԫ�ص����ʵ���______��
��3��������M����������������Ҫ��;��д������Fת��Ϊ����M�Ļ�ѧ����ʽ��______��
����ҺD��ͨ��______CO2���ɳ���F�����ӷ���ʽΪ��______��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com