
| A. | 1:1 | B. | 2:1 | C. | 3:1 | D. | ≧3:1的任意比 |
分析 通入饱和碳酸氢钠溶液,发生反应:3NO2+H2O=2HNO3+NO,HNO3+NaHCO3=NaNO3+CO2↑+H2O,总反应方程式为:3NO2+2NaHCO3=2NaNO3+NO↑+2CO2↑+H2O,气体总体积不变为7mL,再通过足量的过氧化钠,发生反应:2CO2+2Na2O2═2Na2CO3+O2,2NO+O2=2NO2,总反应方程式为:CO2+NO+Na2O2═Na2CO3+NO2,气体的体积被3.5mL,则通过碳酸氢钠溶液后混合气体中CO2、NO体积之比满足≥1:1即可.
解答 解:通入饱和碳酸氢钠溶液,发生反应:3NO2+H2O=2HNO3+NO,HNO3+NaHCO3=NaNO3+CO2↑+H2O,总反应方程式为:3NO2+2NaHCO3=2NaNO3+NO↑+2CO2↑+H2O,气体总体积不变为7mL,
再通过足量的过氧化钠,发生反应:2CO2+2Na2O2═2Na2CO3+O2,2NO+O2=2NO2,总反应方程式为:CO2+NO+Na2O2═Na2CO3+NO2,气体的体积被3.5mL,则通过碳酸氢钠溶液后混合气体中CO2、NO体积之比满足≥1:1即可,
假设原混合气体中NO2为x mL,NO为y mL,则:
3NO2+2NaHCO3=2NaNO3+NO↑+2CO2↑+H2O
3 1 2
x mL $\frac{1}{3}$x mL $\frac{2}{3}$x mL
故$\frac{\frac{2}{3}x}{y+\frac{1}{3}x}$≥1:1,
整理可得$\frac{x}{y}$≥$\frac{3}{1}$,
故选:D.
点评 本题考查混合物有关计算,题目涉及转化过程多,属于易错题目,注意总反应方程式的运用,侧重考查学生分析计算能力,难度较大.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| 实验 | 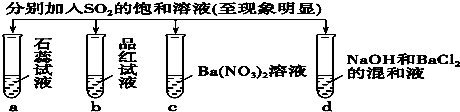 | ||||
| 记录 | A | 无色 | 无色 | 无现象 | 无色溶液 |
| B | 红色 | 无色 | 白色沉淀 | 白色沉淀 | |
| C | 红色 | 无色 | 无色溶液 | 白色沉淀 | |
| D | 无色 | 无色 | 无色溶液 | 无色溶液 | |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
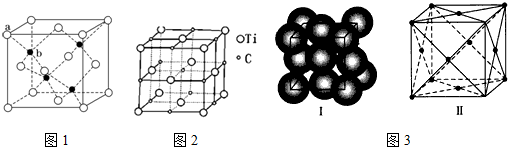
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1个 | B. | 2个 | C. | 3个 | D. | 4个 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
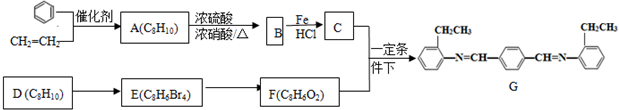

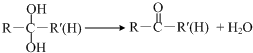
 +CH2=CH2$\stackrel{催化剂}{→}$
+CH2=CH2$\stackrel{催化剂}{→}$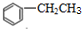 .
.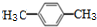 +4Br2$\stackrel{催化剂}{→}$
+4Br2$\stackrel{催化剂}{→}$ 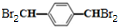 +4HBr.
+4HBr.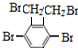 、
、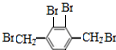 、
、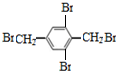 等(仅写3种).
等(仅写3种).查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 周期表中有八个主族,八个副族 | |
| B. | 目前使用的元素周期表中,最长的周期含有32种元素 | |
| C. | 短周期元素是指1-20号元素 | |
| D. | 原子的最外层电子数都等于该元素所在的族序数 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
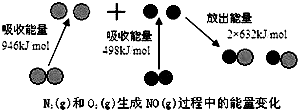
| A. | 1 mol N2(g)和1 mol O2(g)反应放出的能量为180 kJ | |
| B. | 通常情况下,N2(g)和O2(g)混合能直接生成NO | |
| C. | 1 mol N2(g)和1 mol O2(g)具有的总能量小于2 mol NO(g)具有的总能量 | |
| D. | NO是一种酸性氧化物,能与NaOH溶液反应生成盐和水 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com