
| A��25 ��ʱ��pH��2��1.0 L H2SO4��Һ�к���H������ĿΪ0.02 NA |
B��0.5 mol�ۻ�(As4S4������ԭ�Ӷ�����8���ӽṹ���ṹ��ͼ)����NA��S��S��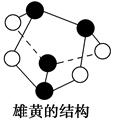 |
| C��39 g�������й���6 NA�����۵��� |
| D����FeI2��NaBr�Ļ����Һ��ͨ����������������1 mol Fe2��������ʱ���÷�Ӧת�Ƶ��ӵ���Ŀ����Ϊ3 NA |

| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A�������£�4g CH4��nA��C��H���ۼ� |
| B��1 mol Fe������ϡHNO3��Ӧ��ת�Ƹ�2nA������ |
| C��1L 0��1 mol/L NaHCO3��Һ�к���0��1nA��HCO3- |
| D�����³�ѹ�£�22��4L��NO2��CO2������庬��2nA��Oԭ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A���ڱ���£�11.2 L NO��11.2 L O2��Ϻ�����������Ϊ0.75NA |
| B�����³�ѹ�£�16 g O3�����ĵ�����Ϊ8NA |
| C��0.1 mol Na2O2�������0.4NA������ |
| D����������������Һ��Ӧ����1 mol����ʱ��ת�Ƶĵ�����ΪNA |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��0.05 mol���ڵ�NaHSO4�к��е���������Ϊ0.10 NA |
| B��25 �棬pH��12��1 L��ˮ�к��е�OH����Ϊ0.01 NA |
| C��11.2 L��ϩ����Ȳ�Ļ�������к��е�̼ԭ����ΪNA |
| D��5.6 g Fe������������ȫ��Ӧ��ת�Ƶĵ�����Ϊ0.3 NA |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��15 g CH3����������Ϊ10 NA |
| B��78 g Na2O2����������ԭ��Ӧ��ת�Ƶ�����һ����NA |
| C��һ�������£����ܱ������г���1 mol N2��3 mol H2��������ѧ��Ӧת�Ƶ�����Ϊ6 NA |
| D��22.4 L(�����)����������������ͭ��һ�������·�����Ӧ��ת�Ƶ�������Ϊ2 NA |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A�����³�ѹ�£�8 g O2����4NA������ |
| B��1 L 0.1 mol��L��1�İ�ˮ����0.1NA��NH4�� |
| C����״���£�22.4 L���Ậ��NA��HCl���� |
| D��1 mol Na����ȫ��������Na2O2��ʧȥ2NA������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A����״���£�2.24 Lˮ��������������ΪNA |
| B��1 L 0.2 mol��L��1��������Һ�к��е�SO42-��Ϊ0.2NA |
| C�����ͱ���������1 mol����ȫȼ������O2�ķ�����Ϊ7.5NA |
| D����״���£�7.1 g����������ʯ�����ַ�Ӧת�Ƶ�����Ϊ0.2NA |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com