
2- 4 |
| A、被还原的硝酸为0.08mol |
| B、反应后溶液中仍有硝酸剩余 |
| C、反应后溶液的pH=1 |
| D、CuS未全部参加反应 |
| 0.48mol |
| (5-2) |
| 0.48mol |
| (5-2) |
| 0.48mol |
| (5-2) |
| 0.05mol |
| 0.05L |


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
| A、水晶、红宝石、珍珠、钻石等装饰品的主要成分都是硅酸盐 |
| B、石油裂解、煤的气化、海水制镁等过程中都包含化学变化 |
| C、有新单质生成的化学反应,一定属于氧化还原反应 |
| D、二氧化硫有漂白、杀菌性能,可在食品加工中大量使用 |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、CH4+Cl2
| |||
B、CH3Cl+Cl2
| |||
C、CH4+2O2
| |||
D、CH2=CH2+H2
|
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、AlCl3溶液和Al2(SO4)3溶液加热、蒸发、浓缩、结晶、灼烧,所得固体的成分相同 |
| B、配制FeCl3溶液时,将FeCl3固体溶解在硫酸中,然后再用水稀释到所需的浓度 |
| C、Na2CO3溶液不可保存在带磨口塞的玻璃瓶中 |
| D、泡沫灭火器中常使用的原料是碳酸钠和硫酸铝 |
查看答案和解析>>
科目:高中化学 来源: 题型:
+ 4 |
2- 4 |
+ 4 |
查看答案和解析>>
科目:高中化学 来源: 题型:
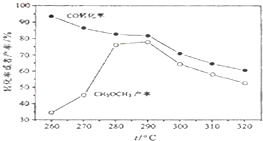 (除零班外其它班做) 一碳化学是国际研究的热点,有研究者在催化剂和压强为5.0MPa的条件下由H2和CO直接制备二甲醚,其反应为:2CO(g)+4H2(g)═CH3-O-CH3(g)+H2O(g),有关图象如图:
(除零班外其它班做) 一碳化学是国际研究的热点,有研究者在催化剂和压强为5.0MPa的条件下由H2和CO直接制备二甲醚,其反应为:2CO(g)+4H2(g)═CH3-O-CH3(g)+H2O(g),有关图象如图:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com