
| A. | 明矾溶于水产生具有吸附性的胶体粒子,可杀菌消毒 | |
| B. | 氯水可使有色布条褪色,说明氯气具有漂白性 | |
| C. | 葡萄糖注射液不能产生丁达尔效应现象,不属于胶体 | |
| D. | 碳素钢和光导纤维都属于新型的无机非金属材料 |
分析 A.氢氧化铝胶体可以吸附杂质,不能杀菌消毒;
B.HClO有漂白性,能漂白某些物质;
C.葡萄糖注射液是溶液;
D.碳素钢属于金属材料,光导纤维属于新型的无机非金属材料.
解答 解:A.明矾水解时产生具有吸附性的氢氧化铝胶体,但氢氧化铝胶体不能杀菌消毒,故A错误;
B.氯水可使有色布条褪色是利用了次氯酸的漂白性,不是氯气的漂白性,故B错误;
C.葡萄糖注射液是溶液,不能产生丁达尔效应现象,不属于胶体,故C正确;
D.碳素钢属于金属材料,不属于新型的无机非金属材料,光导纤维属于新型的无机非金属材料,故D错误;
故选:C.
点评 本题考查了物质的分类与用途,把握物质的性质是解本题关键,性质决定用途,用途体现性质,侧重于考查学生对基础知识的应用能力.


科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
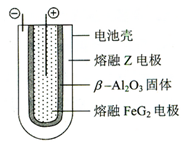 X、Y、Z、M、G五种主族元素分属三个短周期,且原子序数依次增大.X、Z同主族,可形成离子化合物ZX;Y、M同主族,可形成MY2、MY3两种分子.请回答下列问题:
X、Y、Z、M、G五种主族元素分属三个短周期,且原子序数依次增大.X、Z同主族,可形成离子化合物ZX;Y、M同主族,可形成MY2、MY3两种分子.请回答下列问题: .
. 2Z+FeG2放电时,电池的正极反应式为Fe2++2e-=Fe:充电时,钠(写物质名称)电极接电源的负极.
2Z+FeG2放电时,电池的正极反应式为Fe2++2e-=Fe:充电时,钠(写物质名称)电极接电源的负极.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原子的原子核都是由质子和中子构成的,核外电子在原子核外分层运动 | |
| B. | 可以根据主族元素原子的电子层数和最外层电子数确定其在周期表中的位置 | |
| C. | 由氟氯两元素在周期表中位置关系推知,氟元素非金属性强于氯元素,所以氢氟酸的酸性应强于盐酸 | |
| D. | 在实际生产中,多在元素周期表的过渡元素区寻找新型半导体材料 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
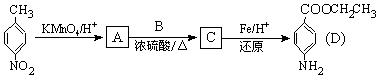
 、BCH3CH2OH、C
、BCH3CH2OH、C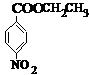 .
.
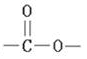
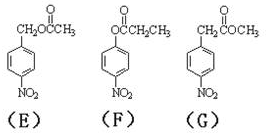
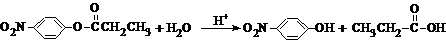 .
.

 的流程图(无机试剂任选).合成路线流程图示如图:
的流程图(无机试剂任选).合成路线流程图示如图:
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1molH2O所含有的原子数为NA | |
| B. | 常温常压下,11.2LCl2所含的分子数为0.5NA | |
| C. | 常温常压下,32g O2含有的氧原子数为2NA | |
| D. | 1L0.1mol/LNa2SO4溶液中所含的Na+为0.1NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氧化性:Br2>Cl2 | B. | 稳定性:HF>HCl | ||
| C. | 碱性:Mg(OH)2>NaOH | D. | 酸性:H2SiO3>H2SO4 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
| A组 | B组 | C组 | D组 | |
| 分类标准 | 非金属单质 | 金属单质 | 金属氧化物 | 酸 |
| 不属于该类的物质 | Al | N2 | SO2 | NH3 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com