
����Ŀ���ռ�ʵ���ҡ��칬һ�š��Ĺ���ϵͳ������������ȼ�ϵ����RFC����RFC��һ�ֽ�ˮ��⼼��������ȼ�ϵ�ؼ������ϵĿɳ���ء���ͼΪRFC����ԭ��ʾ��ͼ���й�˵����ȷ������ ��
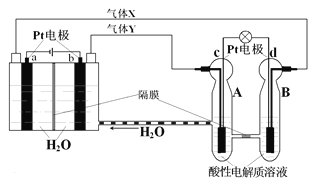
A��ת��0��1mol����ʱ��a�缫����1��12LH2��
B��b�缫�Ϸ����ĵ缫��Ӧ�ǣ�2H2O+2e����H2��+2OH��
C��c�缫��������ԭ��Ӧ��B����е�H+����ͨ����Ĥ����A��
D��d�缫�Ϸ����ĵ缫��Ӧ�ǣ�O2+4H��+4e����2H2O
���𰸡�C
��������
�������������ͼʾ֪���װ���ǵ��أ��ұ�װ����ԭ��أ�a��b�缫�ǵ��صĵ缫���ɵ�Դ�ж�aΪ����������������������bΪ����������������������c��d�缫��ԭ��ص���������c��������d�Ǹ����������еĵ缫��ӦΪ��b�缫Ϊ����ʧ���ӷ���������Ӧ��4OH - -4e - ��2H 2 O+O 2 ����a�缫Ϊ�����õ����ӷ�����ԭ��Ӧ��4H + +4e - ��2H 2 ����ԭ�������������Һ���缫��ӦΪ��dΪ����ʧ���ӷ���������Ӧ��2H 2 -4e - ��4H + ��c�缫Ϊ�����õ����ӷ�����ԭ��Ӧ��O 2 +4H + +4e - ��2H 2 O����A.û�б����������A������B��bΪ����������������������ʧ���ӣ�B����ȷ��C��c�缫Ϊ�����õ����ӷ�����ԭ��Ӧ��O 2 +4H + +4e - ��2H 2 O����Һ��H+�������ƶ���C��ȷ��D�� dΪ����ʧ���ӷ���������Ӧ��2H 2 -4e - ��4H + ��D������


 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��4���������������Ԫ�ص����λ�����,Ԫ��x��ԭ�Ӻ����������m��2��,y��������������ԡ�
m | n | ||
x | y |
�ش���������:
��1��Ԫ��x�����ڱ��е�λ���� ,�䵥�ʿɲ��õ������ �ķ����Ʊ���
��2��������ӣ�mn��2�ĵ���ʽΪ ,��mn��2��Ϊ��±��,������±������,��������������Һ��Ӧ�Ļ�ѧ����ʽΪ ��
��3����֪�軯�ƣ�NaCN��,������ܶ�����γ������,��˹�ҵ�ϲ����軯����������ϡ���軯����Һ���������˵Ľ��ʯ,ͨ�����,ʹ���ʯ�еĽ����ܽ�,����������ˮ�������Na[Au��CN��2],�䷴Ӧ����ʽΪ:��4Au+8NaCN+2H2O+O2=4Na[Au��CN��2]+4NaOH��Na[Au��CN��2]��ˮ��Һ�еĵ��뷽��ʽΪ:��Na[Au��CN��2]=Na++[Au��CN��2]-��Ȼ������п����Һ�аѽ��û�����,пת��ΪNa2[Zn��CN��4]���ݴˣ���������д���ڿ��������軯����Һ��ȡ��ĵ缫��Ӧʽ:����: ������: ��
��4�����˲����軯���ж�,����Na2S2O3����,���߷�Ӧ�õ����ֺ���Ԫ�ص�����,����һ������Fe3+�ɱ�Ϊ��ɫ��д���ⶾԭ����������ӷ���ʽ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����1����֪�����£�Ksp[Fe(OH)3]=4.0��10-38����FeCl3��Һ�м���NaHCO3��Һ�������������壬��Ӧ�����ӷ���ʽΪ��__________��������������Һ��pH����Ϊ4������Һ��Fe3+Ũ��Ϊ__________molL-1
��2����֪ˮ��������ƽ�⣺H2OH++OH-��H��0������ʹƽ�������ƶ�����������Һ�Լ��ԣ�ѡ����__________��
A����ˮ�м���NaHSO4����
B����ˮ�м�Na2CO3����
C��������100��[����c(H+)=1��10-6 molL-1]
D����ˮ�м���NH4Cl����
��3�������£�Ũ�Ⱦ�Ϊ0.1molL-1����������������Һ��pH���±���
���� | CH3COONa | NaHCO3 | Na2CO3 | NaClO | NaCN |
pH | 8.8 | 9.7 | 11.6 | 10.3 | 11.1 |
��������Һ�е������ӣ����H+������ǿ����__________�����ݱ������ݣ�Ũ�Ⱦ�Ϊ0.01molL-1���������������Һ�ֱ�ϡ��100����pH�仯������__________(����)��
A��HCN B��HClO C��CH3COOH D��H2CO3
��4������˵������ȷ����(����š�____________��
A��ij�¶��´�ˮ�е�c(H+)=10-6������������
B����ϡ����ϴ��AgCl��������ˮϴ�����AgClС
C����ͬ�¶��£�0.1mol/LNH4Cl��Һ��NH4+��Ũ�ȱ�0.1mol/L��ˮ��NH4+��Ũ�ȴ�
D����ͬ�¶���pH��Ϊ8 ��Na2CO3��NaHCO3��Һ��ǰ�����ʵ���Ũ�ȴ�
E����ʯ��ˮ�м���CaO���壬��Һ��Ca2+��OH-�����ʵ�������С
��5��ʵ�����г���NaOH������ϴ�����ᴿ����400mL 1molL-1��NaOH��Һ���ձ�״����4.48LCO2ʱ��������Һ�и�����Ũ���ɴ�С��˳��Ϊ__________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����и������������FeƬ��ʴ�ɿ쵽����˳����( )
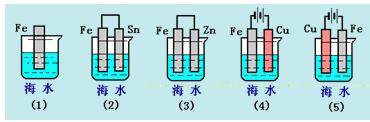
A��(5)(2)(1)(3)(4) B��(2)(5)(3)(4)(1)
C��(5)(3)(4)(1)(2) D��(1)(5)(3)(4)(2)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����Ļ�����ϳɡ�Ӧ�ü����Ĺ̶�һֱ�ǿ�ѧ�о����ȵ㡣
��1����CO2��NH3Ϊԭ�Ϻϳɻ������ص���Ҫ��Ӧ���£�
��2NH3��g����CO2��g����NH2CO2NH4��s������H����159.47 kJ��mol��1
��NH2CO2NH4��s����CO ��NH2��2��s����H2O��g������H��a kJ��mol��1
��2NH3��g����CO2��g����CO��NH2��2��s����H2O��g������H����86.98 kJ��mol��1��aΪ ��
��2����Ӧ2NH3��g����CO2��g��![]() CO��NH2��2��l����H2O��g�� �ںϳ����н��С���ͼ�Т���������Ϊ�ϳ����а���ͬ��̼�� [n��NH3��/n��CO2��]��ˮ̼��[n��H2O��/n��CO2��]Ͷ��ʱ������̼ת���ʵ������
CO��NH2��2��l����H2O��g�� �ںϳ����н��С���ͼ�Т���������Ϊ�ϳ����а���ͬ��̼�� [n��NH3��/n��CO2��]��ˮ̼��[n��H2O��/n��CO2��]Ͷ��ʱ������̼ת���ʵ������

�����ߢ�ˮ̼�ȵ���ֵ�ֱ�Ϊ��
A��0.6��0.7 B��1��1.1 C��1.5��1.61
������Ӧѡ��ˮ̼�ȵ���ֵΪ ��ѡ����ţ���
�������а�̼���˿�����4.0���ң�������4.5��ԭ������� ��
��3�����ؿ�����ʪ�������ѵ����գ��䷴Ӧԭ��Ϊ��
NO��NO2��H2O��2HNO2��2HNO2��CO��NH2��2��2N2����CO2����3H2O��
�ٵ�������NO��NO2��������Ӧ��ϵ����ʱ�ѵ�Ч����ѡ���������V��NO����V��NO2����5��1ʱ����ͨ��һ�����Ŀ�����ͬ��ͬѹ�£�V����������V��NO���� �����������������������ԼΪ20%����
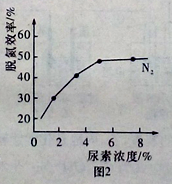
��ͼ2�����غ������ѵ�Ч�ʵ�Ӱ�죬�Ӿ��������Ͽ��ǣ�һ��ѡ������Ũ��ԼΪ %��
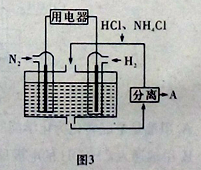
��4��ͼ3��ʾʹ�����͵缫���ϣ���N2��H2Ϊ�缫��Ӧ���HCl��NH4ClΪ�������Һ����������ṩ������ͬʱ����ʵ�ֵ��̶�������ȼ�ϵ�ء���д���õ�ص�������Ӧʽ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪A(g)+B(g) ![]() C(g)+D(g)��Ӧ��ƽ�ⳣ�����¶ȵĹ�ϵ���£�
C(g)+D(g)��Ӧ��ƽ�ⳣ�����¶ȵĹ�ϵ���£�
�¶�/ �� | 700 | 800 | 830 | 1000 | 1200 |
ƽ�ⳣ�� | 1.7 | 1.1 | 1.0 | 0.6 | 0.4 |
830��ʱ����һ��2 L���ܱ������г���0.2mol��A��0.8mol��B����Ӧ��ʼ4 s��A��ƽ����Ӧ����v(A)=0��005 mol/(L��s)������˵����ȷ����
A��4 sʱc(B)Ϊ0.76 mol/L
B��830����ƽ��ʱ��A��ת����Ϊ80%
C����Ӧ��ƽ��������¶ȣ�ƽ�������ƶ�
D��1200��ʱ��ӦC(g)+D(g) ![]() A(g)+B(g)��ƽ�ⳣ����ֵΪ0.4
A(g)+B(g)��ƽ�ⳣ����ֵΪ0.4
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵����ȷ����
A. ij��Һ![]() ���ɰ�ɫ������˵��ԭ��Һ����Cl-
���ɰ�ɫ������˵��ԭ��Һ����Cl-
B. ij��Һ![]() ���ɰ�ɫ������˵��ԭ��Һ����SO42-
���ɰ�ɫ������˵��ԭ��Һ����SO42-
C. ij��Һ![]() ������ɫ���壬˵��ԭ��Һ����CO32-
������ɫ���壬˵��ԭ��Һ����CO32-
D. ij��Һ![]() ������ɫ������˵��ԭ��Һ����Cu2+
������ɫ������˵��ԭ��Һ����Cu2+
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ϴ�Ӽ��㷺�������ǵ������У�����ϴ��������ϴ�Ӽ������黯���ܵ���
A�������ͳ�ȥ�·��ϵ�����
B���ò;�ϴ�ྫ��ϴ�;��ϵ�����
C����ˮϴȥ�����е�ˮ����
D���ô�ϴȥˮ����ˮ��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com