
已知多硫化钠Na2Sx(x≥2)在碱性溶液中可被NaClO氧化为Na2SO4,而NaClO被还原为NaCl,反应中Na2Sx与NaClO的物质的量之比为1:10,则x值是()
A. 2 B. 3 C. 4 D. 5
考点: 氧化还原反应的计算.
专题: 氧化还原反应专题.
分析: Na2Sx在碱性溶液中可被NaClO氧化为Na2SO4,S元素化合价由﹣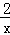 升高为+6,而NaClO被还原为NaCl,Cl元素化合价由+1价降低为﹣1价,反应中Na2Sx与NaClO的物质的量之比为1:10,根据氧化还原反应中转移电子相等进行解答.
升高为+6,而NaClO被还原为NaCl,Cl元素化合价由+1价降低为﹣1价,反应中Na2Sx与NaClO的物质的量之比为1:10,根据氧化还原反应中转移电子相等进行解答.
解答: 解:Na2Sx在碱性溶液中可被NaClO氧化为Na2SO4,S元素化合价由﹣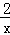 升高为+6,而NaClO被还原为NaCl,Cl元素化合价由+1价降低为﹣1价,反应中Na2Sx与NaClO的物质的量之比为1:10,则:
升高为+6,而NaClO被还原为NaCl,Cl元素化合价由+1价降低为﹣1价,反应中Na2Sx与NaClO的物质的量之比为1:10,则:
x×[6﹣(﹣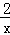 )]=10×[1﹣(﹣1)],即x(6+
)]=10×[1﹣(﹣1)],即x(6+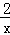 )=20,
)=20,
解得x=3,
故选B.
点评: 本题考查了氧化还原反应,根据氧化还原反应中转移电子相等进行计算即可,难度不大.


科目:高中化学 来源: 题型:
1体积pH=2.5的盐酸与10体积某一元强碱溶液恰好完全反应,是该碱溶液的pH等于( )
|
| A. | 9.0 | B. | 9.5 | C. | 10.5 | D. | 11.0 |
查看答案和解析>>
科目:高中化学 来源: 题型:
由铜、锌和稀硫酸组成的原电池中(图1):
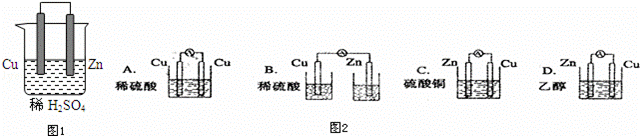
(1)锌是负极,电极反应式是 .铜是正极,电极反应式是 .总反应式
(2)在铜极上可以观察到 ,在锌极可以观察到 (填实验现象)
(3)图2装置能够组成原电池是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
下列各组离子能在指定溶液中大量共存的一组是()
A. 在稀盐酸中:Ba2+、CO32﹣、Zn2+
B. 在氢氧化钠溶液中:H+、Mg2+、Cl﹣
C. 在硫酸铵溶液中:Na+、K+、OH﹣
D. 在氯化钠溶液中:K+、Ca2+、N03﹣
查看答案和解析>>
科目:高中化学 来源: 题型:
在两个密闭容器中,分别充有质量相同的甲乙两种气体,若它们的温度和密度均相同,试根据甲、乙的摩尔质量(M)关系,判断下列说法正确的是()
A. 若M(甲)>M(乙),则气体体积:甲<乙
B. 若M(甲)<M(乙),则气体压强:甲>乙
C. 若M(甲)>M(乙),则气体的摩尔体积:甲>乙
D. 若M(甲)<M(乙),则分子数:甲<乙
查看答案和解析>>
科目:高中化学 来源: 题型:
Ⅰ.现欲用该浓硫酸配制成1mol/L的稀硫酸.现实验室仅需要这种稀硫酸220mL.试回答下列问题:
(1)用量筒量取该浓硫酸 mL.
(2)配制时,必须使用的仪器除量筒、烧杯外,还缺少的仪器是 .
(3)若在稀释过程中,浓硫酸不慎沾在手上,处理方法为 .
(4)配制溶液的过程中,其他操作都正确,下列操作会使所配溶液浓度偏高的是BCF.
A.用量筒量取浓硫酸时俯视
B.稀释浓硫酸时,未冷却到室温即转移到容量瓶中
C.量取浓H2SO4后的量筒进行洗涤,并将洗涤液转移到容量瓶中.
D.定容摇匀后,发现液面低于刻度线,又用胶头滴管加蒸馏水至凹液面最低处与刻度线相切
E.容量瓶不干燥
F.定容时,俯视容量瓶刻度线
Ⅱ.
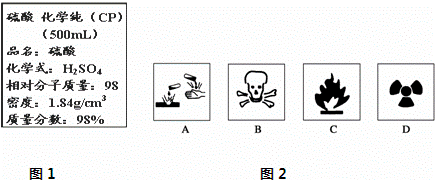
(1)在盛放浓硫酸的试剂瓶的标签上应印有图2警示标志中的A.
(2)若将该浓硫酸与等质量的水混合,则所得溶液中溶质物质的量浓度 9.2mol/L(填>、<、=)
查看答案和解析>>
科目:高中化学 来源: 题型:
工业上制备纯硅反应的热化学方程式如下:SiCl4(g)+2H2(g)⇌Si(g)+4HCl(g);△H=+Q kJ•mol﹣1(Q>0),某温度、压强下,将一定量反应物通入密闭容器进行以上反应,下列叙述 正确的是()
正确的是()
A. 反应过程中,若增大压强能提高SiCl4的转化率
B. 若反应开始时SiCl4为1mol,则达平衡时,吸收热量为Q kJ
C. 反应至4min时,若HCl浓度为0.24 mol/L,则H2的反应速率为0.03 mol/(L•min)
D. 当反应吸收热量为0.025Q kJ时,生成的HCl通入100mL 1mol•L﹣1的NaOH溶液恰好反应
查看答案和解析>>
科目:高中化学 来源: 题型:
下列实验操作中现象、结论均正确的是( )
| 操作 | 现象 | 结论 | |
| A | 甲和乙用导线连接插入稀盐酸溶液中 | 乙溶解,甲上有H2气放出 | 金属甲比乙活泼性强 |
| B | 向一无色溶液中滴加氯水和CCl4,振荡、静置 | 上层溶液显紫色 | 原溶液中有I﹣ |
| C | 用洁净铂丝蘸取溶液进行焰色反应 | 火焰呈黄色 | 原溶液中有Na+,无K+ |
| D | 向一定浓度的Na2SiO3溶液中通入适量CO2气体 | 出现白色沉淀 | H2SiO3的酸性比H2CO3弱 |
|
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com