
 (1)配制0.5mol/L的NaOH溶液,定容时向容量瓶中加蒸馏水超过刻度线,其结果偏小.(填“偏大”、“偏小”、或“不变”)
(1)配制0.5mol/L的NaOH溶液,定容时向容量瓶中加蒸馏水超过刻度线,其结果偏小.(填“偏大”、“偏小”、或“不变”)分析 (1)根据c=$\frac{n}{V}$并结合溶质的物质的量n和溶液的体积V的变化来进行误差分析;
(2)从石油中分离出汽油、煤油和柴油等的操作为石油的分馏;
(3)根据CO2与饱和NaHCO3溶液不反应,而HCl能与饱和NaHCO3溶液生成CO2来分析;
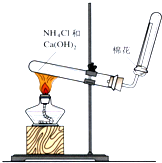
(4)①氨气的密度比空气的小;
②根据氨气是唯一的碱性气体来分析.
解答 解:(1)配制0.5mol/L的NaOH溶液,定容时向容量瓶中加蒸馏水超过刻度线,会导致溶液体积偏大,则浓度偏小,故答案为:偏小;
(2)根据石油中各组分的沸点不同从石油中分离出汽油、煤油和柴油等的操作为石油的分馏,故答案为:分馏;
(3)CO2和HCl均为酸性气体,均能与NaOH溶液反应,而CO2与饱和NaHCO3溶液不反应,而HCl能与饱和NaHCO3溶液生成CO2,故除去二氧化碳气体中的氯化氢杂质,选用的试剂是饱和NaHCO3溶液,故答案为:饱和NaHCO3溶液;
(4)①氨气的密度比空气的小,故采用向下排空气法,故答案为:向下;
②氨气是唯一的碱性气体,故只要能证明有碱性气体逸出,则氨气已集满,故方法为用湿润的红色石蕊试纸靠近塞棉花的试管口,若试纸变蓝色,说明收集满,故答案为:用湿润的红色石蕊试纸靠近塞棉花的试管口,若试纸变蓝色,说明收集满.
点评 本题考查了配制溶液时的误差分析以及气体的除杂,应注意的是CO2与饱和NaHCO3溶液不反应,而HCl能与饱和NaHCO3溶液生成CO2,故除去二氧化碳气体中的氯化氢杂质,选用的试剂是饱和NaHCO3溶液.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:解答题
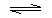 NH3•H2ONH3•H2O
NH3•H2ONH3•H2O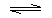 NH4++OH-
NH4++OH-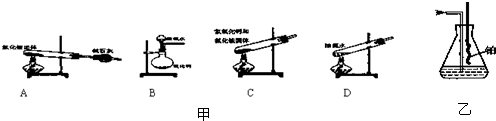
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 4种 | B. | 8种 | C. | 16种 | D. | 40种 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
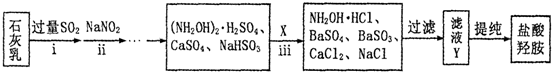
 ;
;
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 将大小、形状相同的镁条和铝条与相同浓度、相同温度下的盐酸反应时,两者快慢相同 | |
| B. | 盛有相同浓度双氧水的两支试管,一支加入MnO2放在冷水中,一支直接放在冷水中,前者反应快 | |
| C. | 将浓硝酸分别放在冷暗处和强光下,发现强光下的浓硝酸分解得快 | |
| D. | 升高温度,H2O2的分解速率加快,原因是反应物分子的能量增加,活化分子百分数增大,有效碰撞次数增多 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
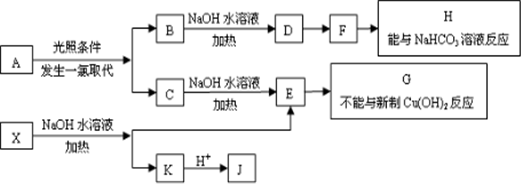
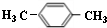 .
.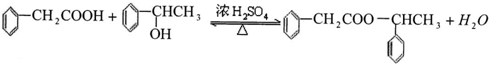 ;该反应类型是酯化反应(或取代反应).
;该反应类型是酯化反应(或取代反应).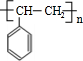 .
.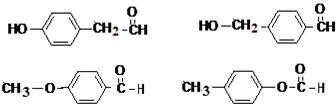 任意一种.
任意一种.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com