
ĻĀĮŠĄė×Ó·½³ĢŹ½ŹéŠ“ÕżČ·µÄŹĒ£ŗ
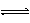 A£®Ģ¼ĖįĒāÄʵÄĖ®½ā£ŗHCO3£+ H2O H3O++ CO32£
A£®Ģ¼ĖįĒāÄʵÄĖ®½ā£ŗHCO3£+ H2O H3O++ CO32£
B£®ŅŌĮņĖįĀĮŗĶŠ”ĖÕ“ņĪŖÖ÷ŅŖ·“Ó¦ĪļµÄÅŻÄĆš»šĘ÷ÖŠµÄ·“Ó¦ŌĄķ£ŗ
Al3+ +3HCO3- ===Al(OH)3”ż£«3CO2”ü
C£®1 mol/L NH4Al(SO4)2ČÜŅŗÖŠÖšµĪ¼ÓČėµČĢå»ż4 mol/L NaOHČÜŅŗ£ŗ
Al3+£«4OH”Ŗ === AlO2££«2H2O
D£®ÓƶčŠŌµē¼«µē½āAlCl3ČÜŅŗ£ŗ2Cl- + 2H2O 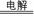 2OH- + H2”ü+ Cl2”ü
2OH- + H2ӟ+ Cl2ӟ

| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ĻĀĮŠ¹ŲÓŚ»ÆѧÓĆÓļµÄ±ķŹ¾ÕżČ·µÄŹĒ (””””)
A£®¹żŃõ»ÆÄʵĵē×ÓŹ½£ŗ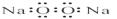
B£®ÖŹ×ÓŹżĪŖ35”¢ÖŠ×ÓŹżĪŖ45µÄäåŌ×Ó£ŗ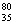 Br
Br
C£®ĀČ»Æļ§”¢“ĪĀČĖį¶¼ŹōÓŚĒæµē½āÖŹ
D£®Ö»µĪ¼Ó°±Ė®¼ų±šNaCl”¢AlCl3”¢MgCl2”¢Na2SO4ĖÄÖÖČÜŅŗ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ŌŚŗ¬ÓŠFe3+”¢Fe2+”¢Al3+”¢NH4+µÄĻ”ČÜŅŗÖŠ£¬¼ÓČė×ćĮæµÄNa2O2¹ĢĢå²¢Ī¢ČČ£¬³ä·Ö·“Ó¦ŗó£¬ŌŁ¼ÓČė¹żĮæµÄĻ”ŃĪĖį£¬ĶźČ«·“Ó¦ŗó£¬Ąė×ÓŹżÄæƻӊĆ÷ĻŌ±ä»ÆµÄŹĒ( )
A.Fe3+ B.Fe2+ C.NH4+ D.Al3+
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ĻÖÓŠĪåÖÖæÉČÜŠŌĪļÖŹA”¢B”¢C”¢D”¢E£¬ĖüĆĒĖłŗ¬µÄŅõ”¢ŃōĄė×Ó»„²»ĻąĶ¬£¬·Ö±šŗ¬ÓŠĪåÖÖŃōĄė×ÓNa£«”¢Al3£«”¢Mg2£«”¢Ba2£«”¢Fe3£«ŗĶĪåÖÖŅõĄė×ÓCl-”¢OH-”¢NO3- ”¢CO32-”¢XÖŠµÄŅ»ÖÖ”£
£Ø1£©Ä³Ķ¬Ń§Ķعż±Č½Ļ·ÖĪö£¬ČĻĪŖĪŽŠė¼ģŃé¾ĶæÉÅŠ¶ĻĘäÖŠ±ŲÓŠµÄĮ½ÖÖĪļÖŹŹĒ
”” ””ŗĶ”” ”””””£
£Ø2£©ĪļÖŹCÖŠŗ¬ÓŠĄė×ÓX”£ĪŖĮĖČ·¶ØX£¬ĻÖ½«£Ø1£©ÖŠµÄĮ½ÖÖĪļÖŹ¼ĒĪŖAŗĶB£¬µ±CÓėBµÄČÜŅŗ»ģŗĻŹ±£¬²śÉśŗģŗÖÉ«³ĮµķŗĶĪŽÉ«ĪŽĪ¶ĘųĢ壻µ±CÓėAµÄČÜŅŗ»ģŗĻŹ±Ņ²²śÉś³Įµķ£¬ĻņøĆ³ĮµķÖŠµĪČėĻ”HNO3£¬³Įµķ²æ·ÖČܽā”£Ōņ£ŗ
¢ŁXĪŖ”” £ØĢī×ÖÄø£©”£
A£®Br- B£®SO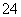 C£®CH3COO- D£®HCO
C£®CH3COO- D£®HCO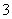
¢ŚAÖŠŅõ”¢ŃōĄė×ÓøöŹż±ČĪŖ
¢ŪBµÄĖ®ČÜŅŗÖŠĖłÓŠĄė×ÓµÄÅضČÓɓ󵽊”µÄĖ³ŠņĪŖ
”””””””” (ÓĆĄė×Ó·ūŗűķŹ¾)”£
¢Ü½«0.02 molµÄAÓė0.01 molµÄCĶ¬Ź±ČܽāŌŚ×ćĮæµÄÕōĮóĖ®ÖŠ£¬³ä·Ö·“Ó¦ŗó£¬×īÖÕĖłµĆ³ĮµķµÄÖŹĮæĪŖ”””””” ””(¾«Č·µ½0.1 g)”£
£Ø3£©½«CuĶ¶Čė×°ÓŠ×ćĮæDČÜŅŗµÄŹŌ¹ÜÖŠ£¬Cu²»Čܽā£»ŌŁµĪ¼ÓĻ”H2SO4£¬CuÖš½„Čܽā£¬¹ÜæŚø½½üÓŠŗģ×ŲÉ«ĘųĢå³öĻÖ£¬ŌņĪļÖŹDŅ»¶Øŗ¬ÓŠÉĻŹöĄė×ÓÖŠµÄ”” £ØĢīĄė×Ó·ūŗÅ£©£¬ÓŠ¹Ų·“Ó¦µÄĄė×Ó·½³ĢŹ½ĪŖ ”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ŌŚµē½āĖ®ÖĘČ”H2ŗĶO2Ź±£¬ĪŖĮĖŌöĒæµ¼µēŠŌ£¬³£³£ŅŖ¼ÓČėŅ»Š©µē½āÖŹ£¬ĻĀĮŠĪļÖŹæÉŃ”ÓĆ£ŗ
A£®NaOH”””””” B£®HC1”””””” C£®NaCl”””””” ””D£®CuSO4
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ĻĀĮŠÓŠ¹ŲĖµ·ØÖŠ£¬²»ÕżČ·µÄŹĒ£ŗ
A£®a mol/LµÄHCNČÜŅŗÓėb mol/LµÄNaOHČÜŅŗµČĢå»ż»ģŗĻ£¬ĖłµĆČÜŅŗÖŠ
c(Na+)>c(CN-)£¬ŌņaŅ»¶ØŠ”ÓŚb
B£®³£ĪĀĻĀ£¬CH3COONaČÜŅŗµÄpH=8£¬Ōņc(Na+) £c(CH3COO-)=9.9”Į10-7mol/L
C£®³£ĪĀĻĀ£¬0.1mol/LµÄijĖįČÜŅŗÖŠ£¬Čōc(OH-)/c(H+) =1”Į10-8£¬ŌņČÜŅŗÖŠÓÉĖ®µēĄė³öµÄ
c(H+) =1”Į10-11mol/L
D£®ŌŚ0.1 mol/L Na2SO3ČÜŅŗÖŠ¼ÓČėÉŁĮæNaOH¹ĢĢ壬c(SO32-)Óėc(Na+)¾łŌö“ó
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ŌŚĻĀĮŠŌŖĖŲÖŠ£¬²»ŹōÓŚÖ÷×åŌŖĖŲµÄŹĒ
A£®Éé B£®īė C£®Ģś D£®µā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
½«SO2ĘųĢåĶØČėBaCl2ČÜŅŗÖŠ£¬Ī“¼ū°×É«³Įµķ£¬¼ĢŠųĶØČėĮķŅ»ÖÖĘųĢåĮ¢¼“²śÉś³Įµķ£¬ŌņĶØČėµÄĘųĢå²»æÉÄܵďĒ
A£®Cl2 B£®NH3 C£®H2S D£®CO2
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
¾ĀČĘųĻū¶¾µÄ×ŌĖ®£¬ČōÓĆÓŚÅäÖĘŅŌĻĀČÜŅŗ£ŗ¢ŁNaOH ¢ŚAgNO3
¢ŪNa2CO3 ¢ÜFeSO4 ¢ŻKI ¢ŽNa2S ¢ßNa2SO3£¬»įŹ¹ÅäÖʵÄČÜŅŗ±äÖŹµÄŹĒ
A.Č«²æ B.¢Ś¢Ü¢Ż¢Ž¢ß C.¢Ł¢Ś¢Ż D.¢Ü¢Ž
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com