
O2和O3是氧元素的两种单质,根据其分子式完成下列各题:
(1)等质量的O2和O3所含分子个数比为________,原子个数比为_________,分子的物质的量之比为_________。
(2)等温等压下,等体积的O2和O3(均为气态)所含分子个数比为___________,原子个数比为___________,质量比为___________。
(3)设NA为阿伏加德罗常数的数值,如果a g氧气中含有的分子数为b,则c g氧气在标准状况下的体积约是___________(用含NA的式子表示)。
(4)配制100 mL 1 mol/L的稀H2SO4溶液,需要用量筒量取浓H2SO4(密度为1.84 g·mL-1,质量分 数为98%)的体积为___________mL。
数为98%)的体积为___________mL。
 捷径训练检测卷系列答案
捷径训练检测卷系列答案 小夫子全能检测系列答案
小夫子全能检测系列答案科目:高中化学 来源:2016-2017学年四川省高二上10月月考化学试卷(解析版) 题型:实验题
某实验小组用0.50 mol·L-1 NaOH溶液和0.50 mol·L-1硫酸溶液进行中和热的测定。
Ⅰ.配制0.50 mol·L-1 NaOH溶液
(1)若实验中大约要使用245 mL NaOH溶液,至少需要称量NaOH固体________g。
(2)从下图中选择称量NaOH固体所需要的仪器(填字母):__________ 。
名称 | 托盘天平(带砝码) | 小烧杯 | 坩埚钳 | 玻璃棒 | 药匙 | 量筒 |
仪器 |
|
|
|
|
|
|
序号 | a | b | c | d | e | f |
Ⅱ.测定稀硫酸和稀氢氧化钠中和热的实验装置如下图所示。
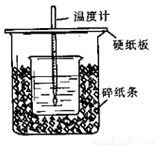
(1)此装置哪些地方需要改进:________________
(2)写出该反应的中和热的热化学方程式(中和热为57.3 kJ·mol-1):__________________
(3)取50 mL NaOH溶液和30 mL硫酸溶液按正确装置进行实验,实验数据如下表。
起始温度/℃ | 终止温度/℃ | 温度差/℃ | |||
H2SO4 | NaOH | 平均值 | |||
1 | 25.5 | 25.0 | 25.25 | 28.5 | 3.25 |
2 | 24.5 | 24.2 | 24.35 | 27.6 | 3.25 |
3 | 25.0 | 24.5 | 24.75 | 26.5 | 1.75 |
①近似认为0.50 mol·L-1 NaOH溶液和0.50 mol·L-1硫酸溶液的密度都是1 g·cm-3,中和后生成溶液的比热容c=4.18 J·g-1·℃-1。则中和热ΔH=_______________(取小数点后一位)。
②上述实验数值结果与57.3 kJ·mol-1有偏差,产生偏差的原因可能是(填字母)____________。
a.实验装置保温、隔热效果差
b.量取NaOH溶液的体积时仰视读数
c.分多次把NaOH溶液倒入盛有硫酸的小烧杯中
d.用温度计测定NaOH溶液起始温度后直接测定H2SO4溶液的温度
(4)如果用50 mL 0.55 mol·L-1的氨水代替NaOH溶液进行上述实验,其放出的热量偏小,原因是________________________
查看答案和解析>>
科目:高中化学 来源:2016-2017学年广西省高一上9月月考化学试卷(解析版) 题型:选择题
某原子的摩尔质量是Mg•mol-1,则一个该原子的真实质量是( )
A.M/6.02×1023 g B.1/M g C.M g D.6.02×1023/M g
查看答案和解析>>
科目:高中化学 来源:2016-2017学年广西省高二上9月月考化学试卷(解析版) 题型:选择题
如图所示,φ(X)为气态反应物在平衡混合物中的体积分数,T为温度.符合该曲线的反应是( )
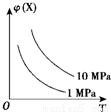
A.N2(g)+3H2(g) 2NH3(g)△H<0
2NH3(g)△H<0
B.2HI(g) H2(g)+I2(g) △H>0
H2(g)+I2(g) △H>0
C.4NH3(g)+5O2(g) 4NO(g)+6H2O(g)△H<0
4NO(g)+6H2O(g)△H<0
D.C(s)+H2O(g) H2(g)+CO(g)△H>0
H2(g)+CO(g)△H>0
查看答案和解析>>
科目:高中化学 来源:2016-2017学年广西省高二上9月月考化学试卷(解析版) 题型:选择题
下图表示反应A(g)+B(g) nC(g);△H<0,在不同条件下反应混合物中C的百分含量和反应过程所需时间的关系曲线。下列有关叙述正确的是( )
nC(g);△H<0,在不同条件下反应混合物中C的百分含量和反应过程所需时间的关系曲线。下列有关叙述正确的是( )
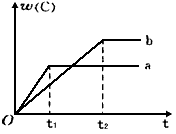
A.反应起始由逆反应开始建立平衡
B.a表示有催化剂,b表示无催化剂
C.若n=2,其它条件相同,a比b的压强大
D.若其它条件相同,a比b的温度高
查看答案和解析>>
科目:高中化学 来源:2016-2017学年宁夏高一上学期期中化学卷(解析版) 题型:选择题
设NA为阿伏加德罗常数,下列关于0.2 mol/L Ba(NO3)2溶液不正确的说法是( )
A.2 L溶液中有阴、阳离子总数为0.8NA
B.500 mL溶液中NO3-浓度为0.4mol/L
C.500 mL溶液中Ba2+浓度为0.2 mol/L
D.500 mL 溶液中NO3-总数为0.2NA
溶液中NO3-总数为0.2NA
查看答案和解析>>
科目:高中化学 来源:2016-2017学年宁夏高一上学期期中化学卷(解析版) 题型:选择题
下列关于纯净物、混合物、电解质、非电解质的正确组合为( )
纯净物 | 混合物[来源 | 电解质 | 非电解质 | |
A | 盐酸 | 冰水混合物 | 硫酸 | 干冰 |
B | 蒸馏水 | 蔗糖溶液 | 氧化铝 | 二氧化硫 |
C | 胆矾 | 盐酸 | 铁 | 碳酸钙 |
D | 胆矾 | 食盐水 | 氯化铜 | 碳酸钠 |
查看答案和解析>>
科目:高中化学 来源:2016-2017学年宁夏高二上学期期中化学卷(解析版) 题型:选择题
在100 mL 0.1 mol·L-1的醋酸溶液中,欲使醋酸的电离程度增大,H+浓度减小,可采用的方法是
A.加热 B.加入100 mL 0.1 mol·L-1的醋酸溶液
C.加入少量的0.5 mol·L-1的硫酸 D.加入少量的1 mol·L-1的NaOH溶液
查看答案和解析>>
科目:高中化学 来源:2016-2017学年内蒙古高二上10月月考化学卷(解析版) 题型:选择题
已知温度T时水的离子积常数为KW,该温度下,将浓度为a mol/L的一元酸HA与b mol/L的一元碱BOH等体积混合,可判定该溶液呈中性的依据是
A.a=b
B.混合溶液的pH=7
C.混合溶液中,c(H+)= 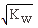 mol/L
mol/L
D.混合溶液中,c(H+)+c(B+)=c(OH-)+c(A-)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com