
碳族元素是形成化合物种类最多的元素。
(1)碳原子2个2p电子的运动状态不相同的方面是_______;C5HxN分子中C、N原于最外层都达到8电子稳定结构,则x的值可能为_______ (选填序号)。
a.10 b.11 c.13 d.15
(2)如图是金刚石晶体的结构示意图。则关于金刚石的描述正确的是 (选填序号)。
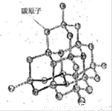
a.C-C键键角都为109°28’ b.最小的环由6个C原子构成
c.可溶于非极性溶剂 d.l mol金刚石含有4 mol C-C键
(3)以下比较错误的是________(选填序号)。
a.稳定性SiH4>CH4 b.沸点SiH4>CH4
c.熔点SiC>Si d.键能C=C>C-C
(4)NaBH4是广泛使用的有机反应还原剂,其中H为-1价,SiO2为其制备原料之一。
①配平以下制备NaBH4的化学方程式:□Na2B4O7+□Na+□SiO2+□H2→□NaBH4+□Na2SiO3
②反应中被还原的元素为________。
(5)碳酸钙是石灰石、方解石等的主要成分,可以形成“喀斯特”地貌、钟乳和石笋,有关反应的化学方程式为_________________________________________。
(6)若物质组成相似,可相互推算组成元素的相对原子质量。某学习小组模拟求算锗的相对原子质量,测得了锗酸钠中Na和Ge的质量分数、硅酸钠中Na和Si的质量分数,他们还需查阅的数据是______(选填序号)。
a.氧元素的相对原子质量
b.硅元素的相对原子质量
c.钠元素的相对原子质量
(1)轨道(或电子云的伸展方向)(1分);bc(2分)
(2)a b(2分)
(3)a.(1分)
(4)①1,16,7,8—4,7(2分);② 0价的H(l分)
(5)CaCO3+CO2+H2O→Ca( HCO3)2(1分)
Ca(HCO3)2 CaCO3↓+CO2↑+H2O(1分)
CaCO3↓+CO2↑+H2O(1分)
(6)b.(1分)
【解析】
试题分析:(1)碳原子2个2p电子分别是x和y轨道上的,运动状态不相同的方面是轨道(或电子云的伸展方向);C5HxN分子中C、N原于最外层都达到8电子稳定结构,分子式可以有C5H10,C5H12,当分子中引入一个氮原子时,可以增加一个氢原子,即分子式可以为C5H11N,C5H13N,则x的值可能为 b.11和c.13。
(2)金刚石晶体是正四面体的空间网状结构,a.C-C键键角都为109°28’,正确; b.最小的环由6个C原子构成,正确;c.可溶于非极性溶剂 ,错误,难溶于任何溶剂中。d.l mol金刚石含有2 mol C-C键,错误;
(3)碳元素的非金属性强于硅,故a.稳定性SiH4>CH4 ,错误;b.由于SiH4相对分子质量大于CH4,分子间作用力较大,故沸点SiH4>CH4,正确;c.两者都是原子晶体,熔点与共价键强弱有关,共价键越短键能越大,熔点越高,由于SiC中键长小于晶体Si中的键长,故熔点SiC>Si ,正确;d.键能C=C>C-C,正确;选a.
(4)NaBH4中B是+3价,H为-1价,化合价发生改变的元素是钠和硼,根据氧化还原反应原理和化合价升降相等,配平如下①1Na2B4O7+16Na+7SiO2+8H2→4NaBH4+7Na2SiO3. ②化合价降低的元素就是被还原的元素为0价的H。
(5)碳酸钙是石灰石、方解石等的主要成分,可以形成“喀斯特”地貌、钟乳和石笋,有关反应的化学方程式为CaCO3+CO2+H2O→Ca(
HCO3)2,Ca(HCO3)2 CaCO3↓+CO2↑+H2O。
CaCO3↓+CO2↑+H2O。
(6)锗酸钠和硅酸钠的组成完全相似,可以通过两者质量分数之比等于它们的相对原子质量之比,要求得锗的相对原子质量,必须要知道 b.硅元素的相对原子质量。
考点:本题考查原子轨道的判断,氧化还原方程式的配平,晶体的性质。


科目:高中化学 来源:物理教研室 题型:021
A. 碳族元素是形成化合物种类最多的一族元素
B. 最高正价与最低负价的绝对值相等的元素一定是碳族元素
C. 碳族元素都是+4价的化合物最稳定
D. 碳族元素的原子半径从上到下依次增大
查看答案和解析>>
科目:高中化学 来源:非常讲解·教材全解全析 高中化学 必修1 (山东版) 山东版 题型:013
|
下列叙述中,正确的是 | |
| [ ] | |
A. |
碳族元素的单质都有导电性 |
B. |
硅酸的酸性比碳酸弱 |
C. |
碳族元素的非金属性比同一周期对应的氧族元素强 |
D. |
碳族元素只能形成共价化合物,不能形成离子化合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:
A.与其他元素化合时易形成共价化合物,难形成离子化合物
B.按原子序数增大的顺序,碳族元素氢化物的稳定性、最高价氧化物对应水化物的酸性都是由强到弱
C.碳族元素单质晶体均为原子晶体,例如金刚石、石墨、晶体硅等
D.碳族元素是形成化合物最多的一族元素
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com