
| Ԫ�� | �����Ӳ�ĵ����� | |||
| K | L | M | N | |
| A | 2 | 7 | ||
| B | 2 | 8 | 1 | |
| C | 2 | 8 | 18 | 7 |
| D | 2 | 8 | 2 | |
| E | 2 | 8 | 7 | |
���� ��1��ͬ����Ԫ�غ�����Ӳ�����ͬ��
��2��ͬ����Ԫ��������������ͬ��
��3���ɺ�������Ų���֪��BΪ��Ԫ�أ��ݴ�д��ѧ����ʽ��
��4��EΪ��������ˮ��Ӧ��������ʹ����ᣮ
��� �⣺��1��B��D��EԪ�ض�����3�����Ӳ㣬����λ��ͬһ���ڣ�
�ʴ�Ϊ��B��D��E��
��2��A��C��E����㶼����7�����ӣ����߶�λ����ͬ���壬
�ʴ�Ϊ��A��C��E��
��3���ɺ�������Ų���֪��BΪ��Ԫ�أ�����ˮ��Ӧ�Ļ�ѧ����ʽΪ��2Na+2H2O=2NaOH+H2����
�ʴ�Ϊ��2Na+2H2O=2NaOH+H2����
��4��EΪ��������ˮ��Ӧ��������ʹ����ᣬ��ѧ����ʽΪ��Cl2+H2O=HCl+HClO��
�ʴ�Ϊ��Cl2+H2O=HCl+HClO��
���� ���⿼��λ�á��ṹ�����ʹ�ϵ��Ӧ�ã���Ŀ�ѶȲ�����ȷԭ�ӽṹ��Ԫ�����ڱ��Ĺ�ϵΪ���ؼ���������ػ���֪ʶ�Ŀ��飬���������ѧ�������Ӧ��������


 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
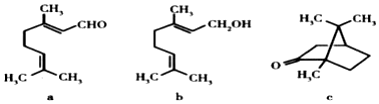
| A�� | ���ֻ�������ֻ��a ��c ��Ϊͬ���칹�� | |
| B�� | һ��������a ��b���ת�� | |
| C�� | ���ֻ�������ױ����� | |
| D�� | ���ֻ�������ɴ��⻯ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
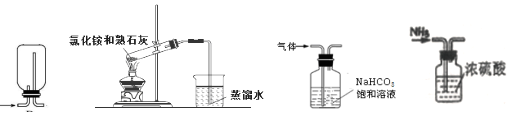
| A�� | �ſ������ռ����� | B�� | �ư�ˮ | ||
| C�� | ��������̼�е������������� | D�� | ����NH3 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
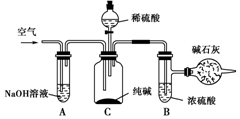 ��ҵ�����г�����NaCl��Na2SO4�����ʣ�������ͼ��ʾ��װ�òⶨ��ҵ��������Ч�ɷֵĺ�����
��ҵ�����г�����NaCl��Na2SO4�����ʣ�������ͼ��ʾ��װ�òⶨ��ҵ��������Ч�ɷֵĺ������鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
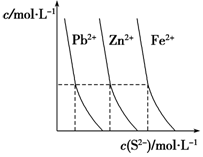 ���л�ѧ�漰��ƽ��������Ҫ��������ѧƽ�⡢����ƽ�⡢ˮ��ƽ����ܽ�ƽ��ȣ������ڹ�ũҵ�����ж��й㷺��Ӧ�ã���ش��������⣺
���л�ѧ�漰��ƽ��������Ҫ��������ѧƽ�⡢����ƽ�⡢ˮ��ƽ����ܽ�ƽ��ȣ������ڹ�ũҵ�����ж��й㷺��Ӧ�ã���ش��������⣺�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | FeCl3 | B�� | Cu2S | C�� | SO3 | D�� | NH3 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��ˮ��ϡ���ᷴӦ | B�� | H2SO4��Al��OH��3��Ӧ | ||
| C�� | ����ʯ��ˮ��ϡ���ᷴӦ | D�� | NaOH��CH3COOH��Һ��Ӧ |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com