
| A. | CaCl2═Ca2++2Cl- | B. | H2SO4═2H++SO42- | ||
| C. | CH3COOH═CH3COO-+H | D. | KOH═K++OH- |
分析 强电解质完全电离,用等号;弱电解质部分电离,用可逆号;电离方程式遵循原子个数、电荷数守恒规律,据此解答.
解答 解:A.氯化钙为强电解质,完全电离,电离方程式:CaCl2═Ca2++2Cl-,故A正确;
B.硫酸为强电解质,完全电离,电离方程式:H2SO4═2H++SO42-,故B正确;
C.醋酸为弱电解质,部分电离,电离方程式:CH3COOH?CH3COO-+H+,故C错误;
D.氢氧化钾为强电解质,完全电离,电离方程式:KOH═K++OH-,故D正确;
故选:C.
点评 本题考查了电解质电离方程式书写,明确电解质强弱及电离方式是解题关键,注意电离方程式遵循原子个数、电荷数守恒规律,题目难度不大.


科目:高中化学 来源: 题型:解答题
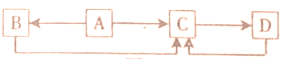
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 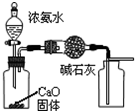 制取并收集干燥纯净的NH3 | |
| B. | 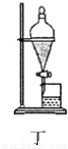 用装置丁分离乙酸乙酯和饱和碳酸钠溶液 | |
| C. | 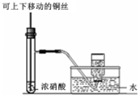 用于制备并收集少量NO2 | |
| D. | 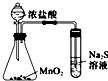 比较MnO2、Cl2、S的氧化性 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
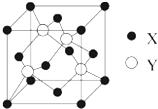 元素X位于第四周期,其基态原子的内层轨道全部排满电子,且最外层电子数为2.元素Y基态原子的3p轨道上有4个电子.元素Z的原子最外层电子数是其内层的3倍.
元素X位于第四周期,其基态原子的内层轨道全部排满电子,且最外层电子数为2.元素Y基态原子的3p轨道上有4个电子.元素Z的原子最外层电子数是其内层的3倍.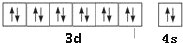
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 铅蓄电池充电时,阳极的反应为:PbSO4+2H2O+2e-═PbO2+SO42-+4H+ | |
| B. | FeCl2溶液与K3[Fe(CN)6]溶液混合后得到特征蓝色沉淀,利用此反应可检验Fe2+ | |
| C. | 常温下将5mL 0.1 mol/LNa2S2O3溶液、5mL 0.01 mol/LNa2S2O3溶液分别与5mL 0.1 mol/LH2SO4溶液混合并搅拌,通过记录溶液中出现浑浊的时间,可确定浓度对化学反应速率的影响 | |
| D. | 处理含有Hg2+离子的废水可加入硫化钠,使Hg2+离子转化为HgS沉淀 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ③ | B. | ①②③ | C. | ③④ | D. | ②③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com