

ЗжЮі ЃЈ1ЃЉЂйвбжЊЃКЂёЃЎN2ЃЈgЃЉ+2H2ЃЈgЃЉЈTN2H4ЃЈlЃЉЁїH=+50.6kJ•mol-1
Ђђ.2H2ЃЈgЃЉ+O2ЃЈgЃЉЈT2H2OЃЈlЃЉЁїH=-571.6kJ•mol-1
ИљОнИЧЫЙЖЈТЩЃЌЂђ-ЂёПЩЕУЃКN2H4ЃЈlЃЉ+O2ЃЈgЃЉЈTN2ЃЈgЃЉ+2H2OЃЈlЃЉЃЛ
ЂкгУДЮТШЫсФЦбѕЛЏАБЃЌПЩвдЕУЕНN2H4ЕФЯЁШмвКЃЌДЮТШЫсФЦБЛЛЙдЩњГЩNaClЃЌЛЙгаЫЎЩњГЩЃЛ
ЃЈ2ЃЉЂйЩ§ИпЮТЖШNH3ЕФШмНтЖШНЕЕЭЃЛ
ЂкбѕЛЏУОФбШмгкЫЎжаЃЌВЛЛсаЮГЩЖўДЮЮлШОЃЛ
ЃЈ3ЃЉЂйИљОнЕчзгзЊвЦЪиКуМЦЫуЯћКФбѕЦјЃЛ
ЂкМзДМКЭNO3-ЗДгІзЊЛЏЮЊСНжжЮоЖОЦјЬхЃЌгІЪЧЩњГЩN2ЁЂCO2ЃЌЗДгІЛЙЩњГЩЫЎЃЛ
ЃЈ4ЃЉдЕчГиИКМЋЗЂЩњбѕЛЏЗДгІЃЌгЩЪОвтЭМПЩжЊЃЌМзДМдкИКМЋЪЇШЅЕчзгЩњГЩCO2гыH+ЃЎ
НтД№ НтЃКЃЈ1ЃЉЂйвбжЊЃКЂёЃЎN2ЃЈgЃЉ+2H2ЃЈgЃЉЈTN2H4ЃЈlЃЉЁїH=+50.6kJ•mol-1
Ђђ.2H2ЃЈgЃЉ+O2ЃЈgЃЉЈT2H2OЃЈlЃЉЁїH=-571.6kJ•mol-1
ИљОнИЧЫЙЖЈТЩЃЌЂђ-ЂёПЩЕУЃКN2H4ЃЈlЃЉ+O2ЃЈgЃЉЈTN2ЃЈgЃЉ+2H2OЃЈlЃЉЃЌдђЁїH=-571.6kJ•mol-1
-50.6kJ•mol-1=-622.2kJ•mol-1ЃЌ
ЙЪД№АИЮЊЃК-622.2ЃЛ
ЂкгУДЮТШЫсФЦбѕЛЏАБЃЌПЩвдЕУЕНN2H4ЕФЯЁШмвКЃЌДЮТШЫсФЦБЛЛЙдЩњГЩNaClЃЌЛЙгаЫЎЩњГЩЃЌЗДгІЗНГЬЪНЮЊЃК2NH3+NaClO=N2H4+NaCl+H2OЃЌ
ЙЪД№АИЮЊЃК2NH3+NaClO=N2H4+NaCl+H2OЃЛ
ЃЈ2ЃЉЂйдк25ЁцЧАЃЌЩ§ИпЮТЖШЕЊШЅГ§ТЪдіДѓЕФдвђЪЧЃКвђЮЊАБЦјШмНтЖШЫцЮТЖШЩ§ИпЃЌШмНтЖШМѕаЁЃЌгаРћгкNH3ЕФвнГіЃЌ
ЙЪД№АИЮЊЃКЩ§ИпЮТЖШNH3ЕФШмНтЖШНЕЕЭЃЌгаРћгкNH3ЕФвнГіЃЛ
ЂкЪЃгрЕФбѕЛЏУОЃЌЪЧФбШмгкЫЎЕФЮяжЪЃЌвдГСЕэЕФаЮЪНХХГіЃЌВЛЛсаЮГЩЖўДЮЮлШОЃЌ
ЙЪД№АИЮЊЃКбѕЛЏУОФбШмгкЫЎжаЃЌвдГСЕэЕФаЮЪНХХГіЃЌвђДЫВЛЛсаЮГЩЖўДЮЮлШОЃЛ
ЃЈ3ЃЉЂй14gяЇЬЌЕЊдЊЫиЮяжЪЕФСПЮЊ$\frac{14g}{14g/mol}$=1molЃЌИљОнЕчзгзЊвЦЪиКуЃЌзЊЛЏЮЊЯѕЬЌЕЊдЊЫиЪБашбѕЕФЮяжЪЕФСПЮЊ$\frac{1molЁС[5-ЃЈ-3ЃЉ]}{4}$=2molЃЌашвЊбѕЦјжЪСПЮЊ2molЁС32g/mol=64gЃЌ
ЙЪД№АИЮЊЃК64gЃЛ
ЂкМзДМКЭNO3-ЗДгІзЊЛЏЮЊСНжжЮоЖОЦјЬхЃЌгІЪЧЩњГЩN2ЁЂCO2ЃЌЗДгІЛЙЩњГЩЫЎЃЌЗДгІРызгЗНГЬЪНЮЊЃК6NO3-+5CH3OH+6H+=3N2Ёќ+5CO2Ёќ+13H2OЃЌ
ЙЪД№АИЮЊЃК6NO3-+5CH3OH+6H+=3N2Ёќ+5CO2Ёќ+13H2OЃЛ
ЃЈ4ЃЉдЕчГиИКМЋЗЂЩњбѕЛЏЗДгІЃЌгЩЪОвтЭМПЩжЊЃЌМзДМдкИКМЋЪЇШЅЕчзгЩњГЩCO2гыH+ЃЌИКМЋЕчМЋЗДгІЪНЮЊЃКCH3OH+H2O-6e-=CO2Ёќ+6H+ЃЌ
ЙЪД№АИЮЊЃКCH3OH+H2O-6e-=CO2Ёќ+6H+ЃЎ
ЕуЦР БОЬтБШНЯзлКЯЃЌЩцМАЗДгІШШМЦЫуЁЂЕчМЋЗДгІЪНЪщаДЁЂбѕЛЏЛЙдЗДгІМЦЫуЕШЃЌЪЧЖдбЇЩњзлКЯФмСІПМВщЃЌФбЖШжаЕШЃЎ



| ФъМЖ | ИпжаПЮГЬ | ФъМЖ | ГѕжаПЮГЬ |
| ИпвЛ | ИпвЛУтЗбПЮГЬЭЦМіЃЁ | ГѕвЛ | ГѕвЛУтЗбПЮГЬЭЦМіЃЁ |
| ИпЖў | ИпЖўУтЗбПЮГЬЭЦМіЃЁ | ГѕЖў | ГѕЖўУтЗбПЮГЬЭЦМіЃЁ |
| ИпШ§ | ИпШ§УтЗбПЮГЬЭЦМіЃЁ | ГѕШ§ | ГѕШ§УтЗбПЮГЬЭЦМіЃЁ |
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃКбЁдёЬт
| AЃЎ | ЂкЂлЂм | BЃЎ | ЂйЂлЂм | CЃЎ | ЂкЂлЂм | DЃЎ | ЂлЂмЂн |
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃКЬюПеЬт
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃКЬюПеЬт
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃКбЁдёЬт
| AЃЎ | MgКЭAl | BЃЎ | MgКЭAg | CЃЎ | NaКЭZn | DЃЎ | FeКЭZn |
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃКбЁдёЬт
| AЃЎ | 25ЁцЪБHAШмвКЕФЕчСІЦНКтГЃЪ§дМЮЊ2ЁС10-6 | |
| BЃЎ | ЕБЕЮШы10mLNaOHЪБШмвКЧЁКУЮЊжаадЃЌдђaЃМ0.5mol•L-1 | |
| CЃЎ | ЕЮМгЙ§ГЬжаЃЌШмвКжаЕФРызгХЈЖШгаПЩФмЮЊcЃЈNa+ЃЉ=cЃЈA-ЃЉ | |
| DЃЎ | ЕЮМгЙ§ГЬжаЃЌШмвКжаЕФРызгХЈЖШЙиЯЕВЛПЩФмгаcЃЈA-ЃЉЃОcЃЈH+ЃЉЃОcЃЈNa+ЃЉЃОcЃЈOH-ЃЉ |
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃКбЁдёЬт
| AЃЎ | ИУШмвКжавЛЖЈВЛКЌK+ЁЂNH4+ЁЂA13+ЁЂSiO32- | |
| BЃЎ | ИУШмвКжавЛЖЈКЌгаA13+ЁЂCO32-ЁЂCl- | |
| CЃЎ | ИУШмвКжаПЩФмКЌгаCl- | |
| DЃЎ | ИУШмвКжавЛЖЈКЌгаK+ЁЂAlO2-ЁЂCO32-ЁЂCl- |
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃКбЁдёЬт
| AЃЎ | жЪСПЯрЕШЕФN2КЭC2H4 | BЃЎ | ЕШЬхЛ§ЕФCOКЭCO2 | ||
| CЃЎ | ЕШЮТЕШЬхЛ§ЕФO2КЭN2 | DЃЎ | ЕШбЙЕШЬхЛ§ЕФN2КЭCO2 |
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃКНтД№Ьт
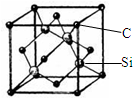 ЭЁЂяиЁЂЮјЁЂЙшЕШдЊЫиЕФЛЏКЯЮяЪЧЩњВњЕкШ§ДњЬЋбєФмЕчГиЕФживЊВФСЯЃЎЧыЛиД№ЃК
ЭЁЂяиЁЂЮјЁЂЙшЕШдЊЫиЕФЛЏКЯЮяЪЧЩњВњЕкШ§ДњЬЋбєФмЕчГиЕФживЊВФСЯЃЎЧыЛиД№ЃКВщПДД№АИКЭНтЮі>>
АйЖШжТаХ - СЗЯАВсСаБэ - ЪдЬтСаБэ
КўББЪЁЛЅСЊЭјЮЅЗЈКЭВЛСМаХЯЂОйБЈЦНЬЈ | ЭјЩЯгаКІаХЯЂОйБЈзЈЧј | ЕчаХеЉЦОйБЈзЈЧј | ЩцРњЪЗащЮожївхгаКІаХЯЂОйБЈзЈЧј | ЩцЦѓЧжШЈОйБЈзЈЧј
ЮЅЗЈКЭВЛСМаХЯЂОйБЈЕчЛАЃК027-86699610 ОйБЈгЪЯфЃК58377363@163.com