
【题目】下列关于有机物的说法正确的是
A.疫苗一般应冷藏存放,目的是避免蛋白质变性
B.分子式为 C3H4Cl2 的同分异构体共有 4 种(不考虑立体异构)
C.有机物呋喃(结构如图所示![]() ),,从结构上看,四个碳原子不可能在同一平面上
),,从结构上看,四个碳原子不可能在同一平面上
D.高分子均难以自然降解
【答案】A
【解析】
A.温度升高,蛋白质会变性,为避免蛋白质变性,疫苗一般应冷藏存放,A正确;
B.C3H6可能是丙烯或环丙烷,环丙烷只有1种氢,判断二氯代物时“定一议一”的方法可确定;丙烯有3种氢,运用相同的方法可确定二氯代物的种类,则同分异构体有:CHCl2CH=CH2、CH2ClCCl=CH2、CH2ClCH=CHCl、CH3CCl=CHCl、CH3CH=CCl2、环丙烷的二氯代物有2种,所以共有7种,B错误;
C.根据乙烯结构,6个原子可能共平面,推出![]() 四个碳原子可能在同一平面上,C错误;
四个碳原子可能在同一平面上,C错误;
D.普通的塑料制品、橡胶、合成纤维等难以自然降解,而可降解塑料在自然界中能降解,D错误。
答案选A。


科目:高中化学 来源: 题型:
【题目】思维辨析:
(1)链状化合物不含碳环,环状化合物不含碳链。(______)
(2)烷烃的官能团是碳碳单键,烯烃的官能团是碳碳双键。(______)
(3)乙酸的分子中含有羧基(![]() )和羟基(—OH)两种官能团。(______)
)和羟基(—OH)两种官能团。(______)
(4)含有相同官能团的有机化合物,一定属于同类物质。(______)
查看答案和解析>>
科目:高中化学 来源: 题型:
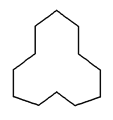
【题目】有机物的结构可以用键线式表示,式中以线示键,每个折点及线端点处表示有一个C原子,并以氢补足四价,C和H不表示出来。
(1)某物质A结构如图所示,其分子式为__________,1 mol该烃完全燃烧需消耗氧气__________mol。
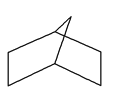
(2)降冰片烷立体结构如图所示,它的分子式为___________;当它发生一氯取代时,取代位置有____种。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用水钴矿(主要成分为Co2O3,含少量Fe2O3、A12O3、MnO、MgO、CaO等)制取草酸钴的工艺流程如图:
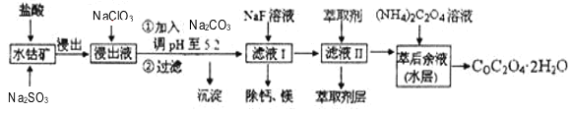
已知:①浸出液含有的阳离子主要有H+、Co2+、Fe2+、Mn2+、Ca2+、Mg2+、Al3+等;
②部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
沉淀物 | Fe(OH)3 | Al(OH)3 | Co(OH)2 | Fe(OH)2 | Mn(OH)2 |
完全沉淀的pH | 3.7 | 5.2 | 9.2 | 9.6 | 9.8 |
(1)浸出过程中加入Na2SO3的目的是_____。
(2)NaClO3在反应中氯元素被还原为最低价,该反应的离子方程式为_____。
(3)加Na2CO3能使浸出液中某些金属离子转化成氢氧化物沉淀。试用离子方程式和必要的文字简述其原理:_____。
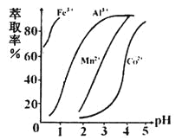
(4)萃取剂对金属离子的萃取率与pH的关系如图所示,在滤液II中适宜萃取的pH为_____左右。
a.2.0~2.5 b.3.0~3.5 c.4.0~4.5
(5)滤液I“除钙、镁”是将其转化为MgF2、CaF2沉淀。已知Ksp(MgF2)=7.35×10-11、Ksp(CaF2)=1.05×10-10,当加入过量NaF后,所得滤液![]() =____。
=____。
(6)工业上用氨水吸收废气中的SO2。已知NH3·H2O的电离平衡常数K=1.8×10-5,H2SO3的电离平衡常数K1=1.2×10-2,K2=1.3×10-8。在通废气的过程中,当恰好形成正盐时,溶液中离子浓度的大小关系为____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将一定量纯净的氨基甲酸铵固体置于恒容的密闭真空容器中,在恒定温度下使其达到分解平衡:NH2COONH4(s) ![]() 2NH3(g)+CO2(g),实验测得不同温度下的平衡数据列于下表:
2NH3(g)+CO2(g),实验测得不同温度下的平衡数据列于下表:
温度/℃ | 15 | 20 | 25 | 30 | 35 |
平衡总压强/kPa | 5.7 | 8.3 | 12.0 | 17.1 | 24.0 |
平衡气体总浓度/ 10-3mol·L-1 | 2.4 | 3.4 | 4.8 | 6.8 | 9.4 |
下列说法正确的是
A. 该反应在低温下可以自发进行
B. 当体系中气体的平均相对分子质量不变时,说明该反应达到了平衡状态
C. 恒温条件下,向容器中再充入2mol NH3和1molCO2,平衡向左移动,平衡后,NH3的浓度减小
D. 15℃时,该反应的平衡常数约为2.05×10-9
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、R、W 均为周期表中前四周期的元素,其原子序数依次增大;X2-和 Y+有相 同的核外电子排布;Z 的氢化物的沸点比其上一周期同族元素氢化物的沸点低;R 的基 态原子在前四周期元素的基态原子中单电子数最多;W 为金属元素,X 与 W 形成的某 种化合物与 Z 的氢化物的浓溶液加热时反应可用于实验室制取 Z 的气态单质。回答下 列问题(相关回答均用元素符号表示):
(1)R 的基态原子的核外电子排布式是__________________。
(2)Z 的氢化物的沸点比其上一周期同族元素氢化物的沸点低的原因是______________。
(3)X 与 Z 中电负性较大的是_____ 。Z 的某种含氧酸盐常用于实验室中 X 的单质的 制取,此酸根离子的空间构型是______________,此离子中含有的化学键类型 是_________ ,X—Z—X 的键角_______109.5°(填“>”、“=”或“<”)。
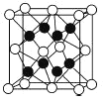
(4)X 与 Y 形成的化合物 Y2X 的晶胞如图。其中 X 离子的配位数 为___________,以相距一个 X 离子最近的所有 Y 离子为顶点构成的几何体为___________ 。该化合物与 MgO 相比,熔点较高的是____________。
(5)已知该化合物的晶胞边长为 a pm,则该化合物的密度为________________g·cm-3(只要求列算式,不必计算出数值,阿伏加德岁常数的数值为 NA)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将29.5 g乙烷和乙烯组成的混合气体缓缓通入足量的溴水后,溴水增重7 g。则原混合气体中,乙烯的体积分数为
A.76%B.50%C.30%D.25%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期元素W、X、Y、Z的原子序数依次递增,a、b、c、d、e、f是由这些元素组成的化合物,d为离子化合物,其结构中还含非极性共价键,m为元素Y的单质,通常为无色无味的气体。上述物质的转化关系如图所示。下列说法正确的是

A. 原子半径:W<X<Y<Z
B. 阴离子的还原性:Y>W
C. a—定由W、X两种元素组成
D. 图中转化过程d物质在作为反应物时均即为氧化剂又是还原剂
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com