
| A£® | ŗĻ³Éøß·Ö×Ó²ÄĮĻ¶¼ÄŃŅŌ½µ½ā£¬»įŌģ³É»·¾³ĪŪČ¾ | |
| B£® | ĖÜĮĻ”¢ĶæĮĻŗĶŗĻ³ÉĻš½ŗ±»³ĘĪŖ”°Čż“óŗĻ³É²ÄĮĻ”± | |
| C£® | Ź³Ę·°ü×°“ü”¢Ź³Īļ±£ĻŹÄ¤µČ²ÄĮĻµÄÖ÷ŅŖ³É·ÖŹĒ¾ŪĀČŅŅĻ© | |
| D£® | ÓĆÓŚÉś²ś”°Äņ²»ŹŖ”±µÄøßĪüĖ®ŠŌŹ÷Ö¬ŹōÓŚ¹¦ÄÜøß·Ö×Ó²ÄĮĻ |
·ÖĪö A”¢²æ·ÖŗĻ³Éøß·Ö×Ó»ÆŗĻĪļÄŃ½µ½ā£»
B”¢ĖÜĮĻ”¢ŗĻ³ÉĻĖĪ¬ŗĶĻš½ŗĪŖČż“óŗĻ³É²ÄĮĻ£»
C”¢Ź³Ę·°ü×°“ü”¢Ź³Īļ±£ĻŹÄ¤µČ²ÄĮĻµÄÖ÷ŅŖ³É·ŻŹĒĀČŅŅĻ©£¬¾ŪĀČŅŅĻ©ÓŠ¶¾£»
D”¢øßĪüĖ®ŠŌŹ÷Ö¬ŹōÓŚ¹¦ÄÜøß·Ö×Ó²ÄĮĻ£®
½ā“š ½ā£ŗA”¢²æ·ÖŗĻ³Éøß·Ö×Ó»ÆŗĻĪļÄŃ½µ½ā£¬Čē¾ŪŅŅĻ©”¢¾ŪĀČŅŅĻ©µČĖÜĮĻÖĘĘ·ÄŃ½µ½ā£¬»įŌģ³É»·¾³ĪŪČ¾£¬µ«²æ·ÖŗĻ³Éøß·Ö×Ó»ÆŗĻĪļŅ×½µ½ā£¬±ČČē£ŗĀĢÉ«Ó«¹āµ°°×ÖŹ£ØGFP£©ŹĒøß·Ö×Ó»ÆŗĻĪļ£¬æɽµ½ā£¬¹ŹA“ķĪó£»
B”¢ĖÜĮĻ”¢ŗĻ³ÉĻĖĪ¬ŗĶĻš½ŗĪŖČż“óŗĻ³É²ÄĮĻ£¬¹ŹB“ķĪó£»
C”¢¾ŪĀČŅŅĻ©ŹÜČČŅ×·Ö½āÉś³ÉÓŠ¶¾ĪļÖŹ£¬ĖłŅŌ¾ŪĀČŅŅĻ©²»ÄÜÓĆĄ“×÷Ź³Ę·°ü×°“ü”¢Ź³Īļ±£ĻŹÄ¤£¬¹ŹC“ķĪó£»
D”¢øßĪüĖ®ŠŌŹ÷Ö¬ŹōÓŚ¹¦ÄÜøß·Ö×Ó²ÄĮĻ£¬¹ŹDÕżČ·£¬¹ŹŃ”D£®
µćĘĄ ±¾Ģāæ¼²éĮĖ»ÆѧÓėÉś»ī£¬×ŪŗĻŠŌ½ĻĒ棬µ«¶¼½Ļ»ł“”£¬×¢Ņā»ł“”ÖŖŹ¶µÄ»żĄŪ£¬²¢ÓĆ»ÆѧÖŖŹ¶½āŹĶÉś²ś”¢Éś»īĻÖĻó£¬ÄŃ¶Č²»“ó£®


 ĢģĢģĻņÉĻŅ»±¾ŗĆ¾ķĻµĮŠ“š°ø
ĢģĢģĻņÉĻŅ»±¾ŗĆ¾ķĻµĮŠ“š°ø Š”ѧɜ10·ÖÖÓÓ¦ÓĆĢāĻµĮŠ“š°ø
Š”ѧɜ10·ÖÖÓÓ¦ÓĆĢāĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 3.0g C2H6ÖŠŗ¬ÓŠ¹²ÓƵē×Ó¶ŌµÄŹżÄæĪŖ0.7”Į6.02”Į1023 | |
| B£® | 25”ꏱpH=1µÄ“×ĖįČÜŅŗÖŠŗ¬ÓŠH+µÄŹżÄæĪŖ0.1”Į6.02”Į1023 | |
| C£® | ŅŃÖŖ2CO£Øg£©+O2£Øg£©?2CO2£Øg£©”÷H=-a kg•mol-1£¬½«2NAøöCOÓėNAøöO2»ģŗĻ£¬³ä·Ö·“Ó¦·Å³öa kJµÄČČĮæ | |
| D£® | 50mL 18.4mol•L-1ÅØĮņĖįÓė×ćĮæĶĪ¢ČČ·“Ó¦£¬Éś³ÉSO2·Ö×ÓŹżÄæĪŖ0.46NA |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | Ķ¬Ź±øıäĮ½øö±äĮæĄ“ŃŠ¾æ·“Ó¦ĖŁĀŹµÄ±ä»Æ£¬ÄÜøüæģµĆ³öÓŠ¹Ų¹ęĀÉ | |
| B£® | Ö»ŗ¬Ņ»ÖÖŌŖĖŲµÄĪļÖŹ£¬Ņ»¶Ø²»ŹĒ»ÆŗĻĪļ£¬µ«ŹĒæÉÄÜŹĒ»ģŗĻĪļ | |
| C£® | ŅĄ¾Ż¶”“ļ¶ūĻÖĻóæɽ«·ÖÉ¢Ļµ·ÖĪŖČÜŅŗ”¢½ŗĢåÓė×ĒŅŗ | |
| D£® | ŅĄ¾ŻCO2”¢SO3”¢SiO2ĪŖĖįŠŌŃõ»ÆĪļ£¬æÉŅŌµĆ³ö½įĀŪ£ŗĖįŠŌŃõ»ÆĪļ¾łĪŖ·Ē½šŹōŃõ»ÆĪļ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® |  Ķ¼ÖŠ£¬²åČėŗ£Ė®ÖŠµÄĢś°ō£¬Ō½ææ½üµ×¶ĖøÆŹ“Ō½ŃĻÖŲ | |
| B£® |  Ķ¼ÖŠ£¬æŖ¹ŲÓÉMøÄÖĆÓŚNŹ±£¬Cu-ZnŗĻ½šµÄøÆŹ“ĖŁĀŹ¼Óæģ | |
| C£® |  Ķ¼ÖŠ£¬½ÓĶØæŖ¹ŲŹ±ZnøÆŹ“ĖŁĀŹŌö“ó£¬ZnÉĻ·Å³öĘųĢåµÄĖŁĀŹŅ²Ōö“ó | |
| D£® |  Ķ¼ÖŠ£¬Zn-MnO2øɵē³ŲĪŖŅ»“ĪŠŌµē³Ų£¬½«NH4Cl»»³ÉŹŖµÄKOHŗóµē³ŲŠŌÄÜøüŗĆ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
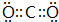 £¬BÓėDŠĪ³ÉµÄŌ×ÓøöŹż±ČĪŖ1£ŗ1µÄ»ÆŗĻĪļµÄµē×ÓŹ½ŹĒ
£¬BÓėDŠĪ³ÉµÄŌ×ÓøöŹż±ČĪŖ1£ŗ1µÄ»ÆŗĻĪļµÄµē×ÓŹ½ŹĒ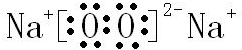 £®
£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | Mg | B£® | Zn2+ | C£® | Fe2+ | D£® | H2 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
 ¼×“¼ŹĒŅ»ÖÖŗÜŗƵÄČ¼ĮĻ£¬¹¤ŅµÉĻÓĆCH4ŗĶH2O£Øg£©ĪŖŌĮĻ£¬Ķعż·“Ó¦IŗĶIIĄ“Öʱø¼×“¼£®
¼×“¼ŹĒŅ»ÖÖŗÜŗƵÄČ¼ĮĻ£¬¹¤ŅµÉĻÓĆCH4ŗĶH2O£Øg£©ĪŖŌĮĻ£¬Ķعż·“Ó¦IŗĶIIĄ“Öʱø¼×“¼£®| ŹµŃ鱹ŗÅ | T£Ø”ę£© | n£ØCO£©/n£ØH2£© | p£ØMPa£© |
| l | 150 | 1/3 | 0.1 |
| 2 | n | 1/3 | 5 |
| 3 | 350 | m | 5 |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com