
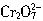 ,这些
,这些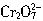 可以从过量的KI溶液中氧化出2.667gI2,反应的离子方程式为:
可以从过量的KI溶液中氧化出2.667gI2,反应的离子方程式为: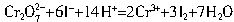
 新活力总动员暑系列答案
新活力总动员暑系列答案 龙人图书快乐假期暑假作业郑州大学出版社系列答案
龙人图书快乐假期暑假作业郑州大学出版社系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
A.K3Cr2Cl7 B.K3Cr2Cl5 C.K3Cr2Cl9 D.K2CrCl4
查看答案和解析>>
科目:高中化学 来源: 题型:
A.K3Cr2Cl9 B.K3Cr2Cl
查看答案和解析>>
科目:高中化学 来源: 题型:
将KCl和CrCl3两种固体混合物共熔发生化合反应制得化合物X。将5.405gX中Cr元素全部氧化成Cr2O72-,酸性的Cr2O72-可与过量的KI发生氧化还原反应氧化出7.62g I2,同时Cr2O72-被还原成Cr3+,如果取溶有X 5.405g的溶液,加入过量的AgNO3,可得12.915gAgCl沉淀。(1)写出Cr2O72-与I-反应的离子方程式
(2)通过计算得出X的化学式
查看答案和解析>>
科目:高中化学 来源:2011-2012学年河南省高三第一次月考化学试卷 题型:计算题
将KCl和CrCl3两种固体混合物共熔发生化合反应制得化合物X。将5.405gX中Cr元素全部氧化成Cr2O72-,酸性的Cr2O72-可与过量的KI发生氧化还原反应氧化出7.62g I2,同时Cr2O72-被还原成Cr3+,如果取溶有X 5.405g的溶液,加入过量的AgNO3,可得12.915gAgCl沉淀。(1)写出Cr2O72-与I-反应的离子方程式
(2)通过计算得出X的化学式
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com