
| 1 |
| 2 |
| 1 |
| 2 |
| 消耗量 |
| 起始量 |
| 1 |
| 2 |
| 1 |
| 2 |
| c(H2)?c(CO2) |
| c(CO)?c(H2O) |
| X2 |
| (0.1-X)2 |
| 0.075 |
| 0.1 |


科目:高中化学 来源: 题型:
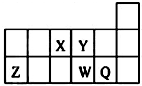 短周期元素X、Y、Z、W、Q在元素周期表中的相对位置如图所示.下列说法不正确的是( )
短周期元素X、Y、Z、W、Q在元素周期表中的相对位置如图所示.下列说法不正确的是( )| A、元素X与元素Z的最高正化合价之和的数值等于8 |
| B、Z的氧化物能与水反应 |
| C、离子Y2-和Z3+的核外电子数和电子层数都相同 |
| D、元素Y的氢化物的稳定性比W的氢化物强 |
查看答案和解析>>
科目:高中化学 来源: 题型:
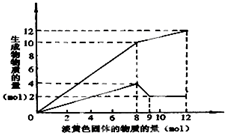 某溶液中可能含有Fe2+、Mg2+、Cu2+、NH4+、Al3+中的一种或几种.当加入一种淡黄色固体并加热溶液时,有刺激性气体放出和白色沉淀生成,加入淡黄色固体的物质的量(横坐标)与析出沉淀和产生气体的物质的量(纵坐标)的关系,如图所示.请填写下列空白:
某溶液中可能含有Fe2+、Mg2+、Cu2+、NH4+、Al3+中的一种或几种.当加入一种淡黄色固体并加热溶液时,有刺激性气体放出和白色沉淀生成,加入淡黄色固体的物质的量(横坐标)与析出沉淀和产生气体的物质的量(纵坐标)的关系,如图所示.请填写下列空白:查看答案和解析>>
科目:高中化学 来源: 题型:

| 实验 序号 | 实验操作 | 现象 |
| Ⅰ | 将氯水滴入品红溶液 | ① |
| Ⅱ | 氯水中加入碳酸氢钠粉末 | 有无色气泡产生 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| 酸或碱 | 电离平衡常数(Ka或Kb) |
| CH3COOH | 1.7×10-5mol?L-1 |
| HNO2 | 7.1×10-4mol?L-1 |
| HCN | 6.2×10-10mol?L-1 |
| HClO | 4.7×10-8mol?L-1 |
| NH3?H2O | 1.7×10-5mol?L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com