
已知反应2KMnO4+16HCl=2KCl+2MnCl2+5Cl2↑+8H2O,若有2.24LCl2(已换算为标准状况)生成,请回答:
(1)HC1在该反应过程中表现出的化学性质有___________。
A.酸性 B.还原性 C.氧化性 D.挥发性
被氧化的HCl为____________g,转移电子数目为_________________。
(2)用“双线桥”或“单线桥”标出上述反应的电子转移方向和数目
 99加1领先期末特训卷系列答案
99加1领先期末特训卷系列答案 百强名校期末冲刺100分系列答案
百强名校期末冲刺100分系列答案 好成绩1加1期末冲刺100分系列答案
好成绩1加1期末冲刺100分系列答案 金状元绩优好卷系列答案
金状元绩优好卷系列答案科目:高中化学 来源:2016届浙江省高三上学期10月阶段测化学试卷(解析版) 题型:选择题
四组同学设计的4个不同喷泉实验方案,下列有关操作不可能引发喷泉现象的是
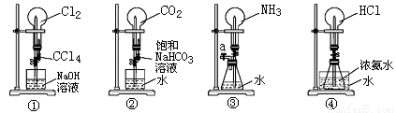
A.挤压装置①的胶头滴管使CCl4全部进人烧瓶,片刻后打开止水夹
B.挤压装置②的胶头滴管使饱和NaHCO3溶液全部进人烧瓶.片刻后打开止水夹
C.用鼓气装置从装置③的a处不断鼓人空气并打开止水夹
D.向装置④的水槽中慢慢加人足量浓硫酸并打开止水夹
查看答案和解析>>
科目:高中化学 来源:2016届甘肃省高三上学期10月月考化学试卷(解析版) 题型:选择题
短周期元素X、Y、Z、W的原子序数依次增大,X的原子在元素周期表中原子半径最小,Y 的次外层电子数是最外层的1/3,ZX2是一种储氢材料,W与Y属于同一主族。下列叙述正确的是
A.原子半径:rW>rZ>rY
B.Y形成的离子与W形成的离子的电子数不可能相同
C.化合物X2Y、ZY、WY3 中化学键的类型相同
D.由X、Y、Z、W组成的化合物的水溶液可能显酸性
查看答案和解析>>
科目:高中化学 来源:2015-2016学年江苏省高二上期中测试化学试卷(解析版) 题型:推断题
(6分)下图是一些常见的单质、化合物之间的转化关系图,有些反应中的部分物质被略去。反应①常被应用于野外焊接钢轨,F是海水中含有盐的主要成分,J为D、G反应产物形成的水溶液。
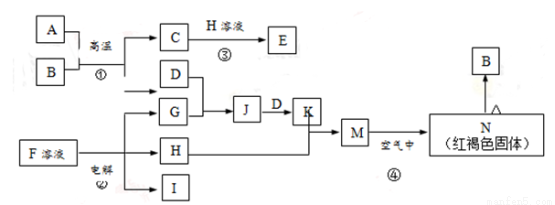
请回答下列问题:
(1)B的化学式为 。
(2)反应②在工业上通常称之为 工业。
(3)写出反应③的离子方程式 。
(4)写出反应④的化学方程式 。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年湖北省高二上第一次月考化学试卷(解析版) 题型:实验题
(10分)用50mL0.50mol/L的盐酸与50mL0.55mol/L的氢氧化钠溶液在如图所示的装置中进行中和反应,通过测定反应过程中所放出的热量可计算中和热。回答下列问题:
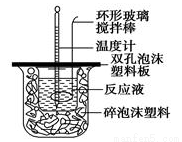
(1)烧杯间填满碎泡沫塑料的作用是 ;
(2)环形玻璃搅拌棒能否用环形铁质搅拌棒代替? (填“能”或“不能”),其原因是 ;
(3)实验时氢氧化钠溶液的浓度要用0.55 mol/L的原因是_______________。
实验中若改用60 mL 0.50 mol/L的盐酸与50 mL 0.55 mol/L的氢氧化钠溶液进行反应, 与上述实验相比,所放出的热量 (填“相等”“不相等”),若实验操作均正确,则所求中和热 (填“相等”“不相等”)。
(4)已知在稀溶液中,强酸和强碱发生中和反应生成1 mol H2O时,放出57.3 kJ的热量,则上述反应的热化学方程式为:___________________。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年安徽省高一上期中测试化学试卷(解析版) 题型:选择题
化学与科学、技术、社会、环境密切相关,下列有关说法中错误的是
A.2010年11月广州亚运会燃放的焰火是某些金属元素焰色反应所呈现出来的色彩
B.小苏打是制作馒头和面包等糕点的膨松剂,还是治疗胃酸过多的一种药剂
C.为防止中秋月饼等富脂食品因被氧化而变质,常在包装袋中放入生石灰或硅胶
D.从海水中制取氯气的过程涉及氧化还原反应
查看答案和解析>>
科目:高中化学 来源:2016届甘肃省高三上学期第一次月考化学试卷(解析版) 题型:填空题
(14分)氯化铁和高铁酸钾都是常见的水处理剂。下图为制备氯化铁及进一步氧化制备高铁酸钾的工艺流程。
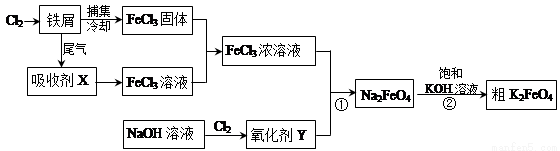
请回答下列问题:
(1)氯化铁有多种用途,请用离子方程式表示下列用途的原理。
①氯化铁做净水剂______________________;(2分)
②用FeCl3溶液(32%~35%)腐蚀铜印刷线路板_________________________。(2分)
(2)吸收剂X的化学式为 ;(1分)氧化剂Y的化学式为____________。(1分)
(3)碱性条件下反应①的离子方程式为____________________________________。(2分)
(4)过程②将混合溶液搅拌半小时,静置,抽滤获得粗产品。该反应的化学方程式为2KOH+Na2FeO4=K2FeO4+2NaOH,请根据复分解反应原理分析反应发生的原因_____ 。(2分)
(5)K2FeO4 在水溶液中易发生反应:4FeO42+10H2O 4Fe(OH)3+8OH+3O2↑。在提纯K2FeO4时采用重结晶、洗涤、低温烘干的方法,则洗涤剂最好选用 (填序号)。(2分)
4Fe(OH)3+8OH+3O2↑。在提纯K2FeO4时采用重结晶、洗涤、低温烘干的方法,则洗涤剂最好选用 (填序号)。(2分)
A.H2O
B.稀KOH溶液、异丙醇
C.NH4Cl溶液、异丙醇
D.Fe(NO3)3溶液、异丙醇
(6)可用滴定分析法测定粗K2FeO4的纯度,有关反应离子方程式为:
①FeO42-+CrO2-+2H2O CrO42-+Fe(OH)3↓+OH-
CrO42-+Fe(OH)3↓+OH-
②2CrO42-+2H+ Cr2O72-+H2O
Cr2O72-+H2O
③Cr2O72-+6Fe2++14H+ 2Cr3++6Fe3++7H2O
2Cr3++6Fe3++7H2O
现称取1.980 g粗高铁酸钾样品溶于适量氢氧化钾溶液中,加入稍过量的KCrO2,充分反应后过滤滤液定容于250 mL容量瓶中。每次取25.00 mL加入稀硫酸酸化,用0.1000 mol/L的(NH4)2Fe(SO4)2标准溶液滴定,三次滴定消耗标准溶液的平均体积为18.93 mL。则上述样品中高铁酸钾的质量分数为 。(2分)
查看答案和解析>>
科目:高中化学 来源:2015-2016学年安徽省高二上学期第一次月考化学试卷(解析版) 题型:填空题
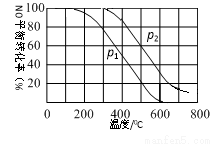
已知Fe(s)+CO2(g) 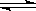 FeO(s)+CO(g) ΔH=a kJ/mol,平衡常数为K;测得在不同温度下,K值如下:
FeO(s)+CO(g) ΔH=a kJ/mol,平衡常数为K;测得在不同温度下,K值如下:
温度/℃ | 500 | 700 | 900 |
K | 1.00 | 1.47 | 2.40 |
(1)该反应的平衡常数表达式K=______________________
(2)方程式中的a________0(填“大于”“小于”或“等于”)。
(3)700℃上述反应达到平衡,要使得该平衡向右移动,其他条件不变时,可以采取的措施有__ ______(填序号)
A.缩小反应器体积 B.通入CO2
C.升高温度到900℃ D.使用合适的催化剂
查看答案和解析>>
科目:高中化学 来源:2015-2016学年江苏省高二上期中选修化学试卷(解析版) 题型:填空题
(10分)NH3经一系列反应可以得到HNO3和NH4NO3,如下图所示。

(1)I中,NH3和O2在催化剂作用下反应,其化学方程式是 。
(2)II中,2NO(g)+O2(g)  2NO2(g) 。起始时容器充入1molNO、0.5molO2,分别测得NO的平衡转化率在不同压强(p1、p2)下随温度变化的曲线(如下图)。
2NO2(g) 。起始时容器充入1molNO、0.5molO2,分别测得NO的平衡转化率在不同压强(p1、p2)下随温度变化的曲线(如下图)。
①比较p1、p2的大小关系 。
②在温度为500℃、压强为p2条件下,平衡混合气中NO2的体积分数 。
(3)III中,将NO2(g)转化成N2O4(l),再制备浓硝酸。
①已知:2NO2(g)  N2O4(g) ΔH1 2NO2(g)
N2O4(g) ΔH1 2NO2(g)  N2O4(l) ΔH2
N2O4(l) ΔH2
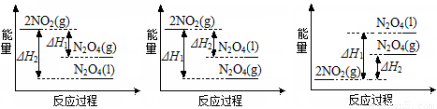
A B C
反应过程中能量变化正确的是 (填序号)。
②N2O4与O2、H2O化合的化学方程式 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com