
由N2O和NO反应生成N2和NO2的能量变化如图所示。下列说法正确的是( )
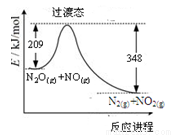
A.断键吸收能量之和大于成键释放能量之和
B.反应物总能量小于生成物总能量
C.N2O(g) +NO(g) =N2(g) +NO2(g)△H= -139kJ/mol
D.反应生成1 mol N2时转移4 mol电子
 小学数学口算题卡脱口而出系列答案
小学数学口算题卡脱口而出系列答案 优秀生应用题卡口算天天练系列答案
优秀生应用题卡口算天天练系列答案 浙江之星课时优化作业系列答案
浙江之星课时优化作业系列答案科目:高中化学 来源:2016-2017学年山东省高二上期中化学卷(解析版) 题型:填空题
含氮化合物在生产、生活和科研中有着广泛的应用。
(1)工业上采用NH3为还原剂处理烟气(假设烟气中的NO和NO2的物质的量相等,且反应产物为无毒气体),测量逸出气体中氮氧化物含量,从而确定烟气脱氮率。如图,下列列说法正确的是(填写下列字母编号)
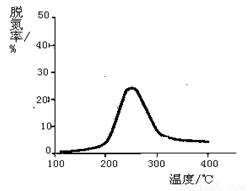
a.相同条件下,改变压强对脱氮率有影响
b.曲线最高点表示此时平衡转化率最高
c.相同条件下,加入不同的催化剂能够改变反应物的转化率
d.上述反应的化学方程式为:NO+NO2+2NH3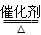 2N2
2N2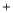 3H2O
3H2O
(2)已知: 2NH3(g)+CO2(g) CO(NH2)2(s)+H2O(g) △H=-43.0KJ·mol-1
CO(NH2)2(s)+H2O(g) △H=-43.0KJ·mol-1
—定条件下,将2molNH3和1molCO2充入容积为2L的密闭容器中发生反应。反应进行2min时,放出热量21.5kJ,则2min内该反应的反应速率υ(NH3)= ,此时混合气体中NH3的体积分数为 。
(3)在25℃下,将a mol•L-1的NH4NO3溶液与0.01mol•L-1的NaOH等体积混合,反应平衡时,测得溶液pH=7,则NH4NO3溶液的物质的量浓度a___________0.01mol•L-1(填“>”、“<”或“=”);滴加NaOH的过程中水的电离平衡将 (填“正向”、“不”或“逆向”)移动。请你设计实验,比较NH3 • H2O的电离程度和NH4NO3的水解程度大小 。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年黑龙江佳木斯一中高一上月考二化学卷(解析版) 题型:选择题
对四组无色透明溶液进行离子检验,四位同学各鉴定一组,他们的实验报告的结论如下,其中可能正确的是
A.Fe3+、K+、I-、Na+ B.Mg2+、NO3-、OH-、Cl-
C.K+、H+、Cl-、CO32- D.Na+、OH-、Cl-、NO3-
查看答案和解析>>
科目:高中化学 来源:2016-2017学年河南省高一12月月考化学卷(解析版) 题型:选择题
下列各组离子,在无色透明溶液中能大量共存的是( )
A.K+、NH4+、Cl?、SO42- B.Ag+、H+、OH?、Cl?
C.Na+、OH?、Cu2+、SO42- D.H+、K+、HCO3?、Cl?
查看答案和解析>>
科目:高中化学 来源:2017届福建省四地六校高三上学期12月月考化学试卷(解析版) 题型:选择题
实验研究发现,金属与硝酸发生氧化还原反应时,硝酸的浓度越稀,对应还原产物中氮元素的化合价越低。现有一定量的铝粉和铁粉 的混合物与足量很稀的硝酸充分反应,反应过程中无气体放出.在反应结束后的溶液中逐滴加入5mol/L NaOH溶液,所加NaOH溶液的体积(mL)与
的混合物与足量很稀的硝酸充分反应,反应过程中无气体放出.在反应结束后的溶液中逐滴加入5mol/L NaOH溶液,所加NaOH溶液的体积(mL)与 产生沉淀的物质的量(mol)关系如图所示,下列说法不正确的是( )
产生沉淀的物质的量(mol)关系如图所示,下列说法不正确的是( )
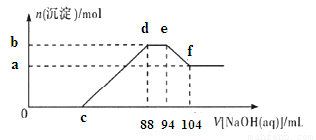
A.稀硝酸与铝粉、铁粉反应,其还原产物为硝酸铵
B.b点与a点的差值为0.05 mol
C.c点对应NaOH溶液的体积为40 mL
D.样品中铝粉和铁粉的物质的量之比为10:9
查看答案和解析>>
科目:高中化学 来源:2017届福建省四地六校高三上学期12月月考化学试卷(解析版) 题型:选择题
25℃时,下列各组离子在指定溶液中一定能大量共存的是( )
A.某无色溶液:Na+、K+、MnO4-、CO32-
B.0.2 mol·L-1 NaNO3溶液中:H+、Fe2+ 、Cl-、SO42-
C.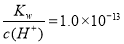 mol·L-1的溶液中:NH4+、Ca2+、Cl-、NO3-
mol·L-1的溶液中:NH4+、Ca2+、Cl-、NO3-
D.使甲基橙变红的溶 液:NH4+、CH3COO-、SO42-、Mg2+
液:NH4+、CH3COO-、SO42-、Mg2+
查看答案和解析>>
科目:高中化学 来源:2017届福建省高三上学期第二次月考化学试卷(解析版) 题型:实验题
有某铁碳合金,某化学兴趣小组为了测定铁碳合金中铁的质量分数,并探究浓硫酸的某些性质,设计了下图所示的实验装置和实验方案(夹持仪器已省略),请你参与此项活动并回答相应问题。

Ⅰ 探究浓硫酸的某些性质
(1)按图示的 连接装置,检查装置的气密性,称量E的质量。
连接装置,检查装置的气密性,称量E的质量。
(2)将m g铁碳合金样品放入A中,再加入适量的浓硫酸。仪器A的名称为________。
未点燃酒精灯前,A、B均无明显现象,其原因是: _。
(3)点燃酒精灯一段时间后,A、B中可观察到明显的现象。
写出A中发生反应的化学方程式_______________________(任写一个)。B中的现象是______________,由此可得到浓硫酸具有____________性。
(4)随着反应的进行,A中还可能发生某些离子反应。写出相应的离子方程式____________(任写一个)。
(5)反应一段时间后,从A中逸出气体的速率仍然较快,除因温度较高,反应放热外,还可能的原因是______________________。
Ⅱ 测定铁的质量分数
(6)待A中不再逸出气体时,停止加热,拆下E并称重。E增重b g。
铁碳合金中铁的质量分数为_____________________(写表达式)。
(7)某同学认为上述方法较复杂,使用下图所示的装置和其它常用实验仪器测定某些数据即可。为了快速和准确的计算出铁的质量分数,最简便的实验操作是___________(填写代号)。
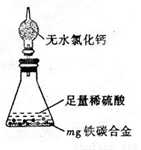
A. 用排水法测定H2的体积
B. 反应 结束后,过滤、洗涤、干燥、称量残渣的质量
结束后,过滤、洗涤、干燥、称量残渣的质量
C. 测定反应前后装置和药品的总质量
查看答案和解析>>
科目:高中化学 来源:2017届福建省高三上学期第二次月考化学试卷(解析版) 题型:选择题
中学化学中很多“规律”都有其使用范围,根据有关“规律”,下列结论合理的
A.根据较强酸可以制取较弱酸的规律,推出CO2通入NaClO溶液中能生成HClO
B.金属镁可以通过电解MgCl2制得,推出金属铝可以通过电解AlCl3制得
C.金属钠在纯氧中燃烧生成Na2O2,推出金属锂在纯氧中燃烧生成Li2O2
D.CaCO3与稀硝酸反应生成CO2,推出CaSO3也能与稀硝酸反应生成SO2
查看答案和解析>>
科目:高中化学 来源:2016-2017陕西西安长安区一中实验班高一12月考化学卷(解析版) 题型:选择题
在Al2(SO4)3 和MgSO4 的混合溶液中,滴加NaOH 溶液,生成沉淀的量与滴入NaOH溶液的体积关系如图所示,则原混合液中 Al2(SO4)3 与MgSO4 的物质的量浓度之比为( )
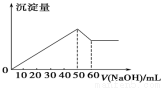
A. 1∶2 B. 2∶1 C. 6∶1 D. 3∶1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com