
����0.8mol��ϡ������Һ����������22.4g������.���跴Ӧ��Ϊ������.��һ��Ϊ��Fe+HNO3![]() Fe(NO3)3+NO��+H2O
Fe(NO3)3+NO��+H2O
(1)д���������η�Ӧ�����ӷ���ʽ.
(2)���������η�Ӧ�У��������۵����ʵ�������Һ����Ԫ�ش��ڵ���ʽ.
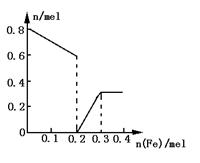
(3)��ͼ�л�����Һ��Fe2+��![]() ���ӵ����ʵ�����������۵����ʵ����仯�Ĺ�ϵͼ��(����������Һ�����ӵ����ʵ���).
���ӵ����ʵ�����������۵����ʵ����仯�Ĺ�ϵͼ��(����������Һ�����ӵ����ʵ���).

(1)Fe+4H++![]()
![]() Fe3++NO��+2H2O
Fe3++NO��+2H2O
2Fe3++Fe![]() 3Fe2+.
3Fe2+.
(2)�ټ���Fe��Ϊ0��0.2molʱ��������ʽΪFe3+.
�ڼ�������Ϊ0.2��0.3molʱ��������ʽΪFe2+��Fe3+
�ۼ�Fe��Ϊn(Fe)��0.3molʱ��������ʽΪFe2+.
(3)����ͼ.
����ϡ���ᷴӦ����
��Fe+4HNO3![]() Fe(NO3)3+NO��+2H2O
Fe(NO3)3+NO��+2H2O
��3Fe+8HNO3![]() 3Fe(NO3)2+2NO��+4H2O
3Fe(NO3)2+2NO��+4H2O
(1)��![]() ��
��![]() ʱ������Ӧ�ٽ��У�
ʱ������Ӧ�ٽ��У�
��![]() ��
��![]() ʱ������Ӧ�ڽ���.
ʱ������Ӧ�ڽ���.
��![]() ��
��![]() ��
��![]() ʱ����٢�����Ӧ����������Fe��HNO3����Ӧ��ȫ.
ʱ����٢�����Ӧ����������Fe��HNO3����Ӧ��ȫ.
(2)������Ӧ������Ϊ�ȷ�����Ӧ�٣���Fe��ʣ������2Fe(NO3)3+Fe![]() 3Fe(NO3)2.
3Fe(NO3)2.



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| ������ | K+��Ag+��Mg2+��Ba2+ | ||||||||
| ������ | NO
|
| ��� | ʵ������ | ʵ���� |
| �� | �����Һ�м�������ϡ���� | ���ɰ�ɫ�������ڱ�״���·ų�0.56L���� |
| �� | �����в����Ļ��Һ���ˣ�������ϴ�ӡ����������أ��������ù�������� | ��������Ϊ2.4g |
| �� | ��������õ���Һ�еμ�BaCl2��Һ | ���������� |
| ������ | NO
|
CO
|
SiO
|
SO
| ||||||||
| c/mol?L-1 | �� �� |
0.25mol/L 0.25mol/L |
0.4mol/L 0.4mol/L |
0 0 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����0.8mol��ϡ������Һ����������22.4g������.���跴Ӧ��Ϊ������.��һ��Ϊ��Fe+HNO3![]() Fe(NO3)3+NO��+H2O
Fe(NO3)3+NO��+H2O
![]() (1)д���������η�Ӧ�����ӷ���ʽ.
(1)д���������η�Ӧ�����ӷ���ʽ.
![]() (2)���������η�Ӧ�У��������۵����ʵ�������Һ����Ԫ�ش��ڵ���ʽ.
(2)���������η�Ӧ�У��������۵����ʵ�������Һ����Ԫ�ش��ڵ���ʽ.
![]() (3)��ͼ�л�����Һ��Fe2+��
(3)��ͼ�л�����Һ��Fe2+��![]() ���ӵ����ʵ�����������۵����ʵ����仯�Ĺ�ϵͼ��(����������Һ�����ӵ����ʵ���).
���ӵ����ʵ�����������۵����ʵ����仯�Ĺ�ϵͼ��(����������Һ�����ӵ����ʵ���).
![]()
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ���¿��� ���ͣ������
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com