
X、Y、Z、W、L、M六种短周期主族元素的原子序数依次增大,其中X、M的单质在常温下呈气态,Y的原子最外层电子数是其电子层数的2倍,Z在同周期的主族元素中原子半径最大,W是地壳中含量最多的金属元素,L的单质晶体熔点高、硬度大,是一种重要的半导体材料.用化学用语回答下列问题:
(1)M的离子结构示意图 ;L在元素周期表中的位置为 .
(2)Y、L、M的最高价含氧酸的酸性由弱到强的顺序是 .
(3)Y的最高价氧化物的电子式为 .原子序数比Y多2的元素的一种氢化物能分解为它的另一种氢化物,此分解反应的化学方程式是 .
(4)Z、W各自的最高价氧化物对应的水化物可以反应生成盐和水,该反应的离子方程式为 .
(5)R与Y同周期,R的单质分子R2中有3个共价键,R与X形成化合物甲,1mol甲含18mol电子,请写出甲的结构式 .
(6)用亚硝酸氧化化合物甲,可生成氮的另一种氢化物,该氢化物的相对分子质量为43,其中氮原子的质量分数为97.7%,该氢化物的分子式为 .该氢化物受撞击时完全分解为氮气和氢气,则2.15g该氢化物受撞击后产生的气体在标况下的体积为 L.
科目:高中化学 来源:2016届辽宁省沈阳市四校协作体高三上学期期中联考化学试卷(解析版) 题型:选择题
化学与科学、社会、技术和环境密切相关。下列有关说法中错误的是
A.目前科学家已制得单原子层锗,其电子迁移率是硅的10倍,有望用于制造高能计算机芯片
B.2014年在西非国家爆发了埃博拉疫情,埃博拉病毒对化学药品敏感,乙醇、次氯酸钠溶液均可以将病毒氧化而达到消毒的目的
C.CO2、CH4、氟氯代烃等都会造成温室效应,因此都属于大气污染物
D.绿色化学期望利用化学原理从源头消除污染,在生产过程中充分利用原料,实现零排放
查看答案和解析>>
科目:高中化学 来源:2015-2016学年福建省高二上学期期中考试化学试卷(解析版) 题型:选择题
在固定容积的密闭容器中,可逆反应2X(?)+Y(g) Z(s)已达到平衡,此时升高温度则气体的密度增大。下列叙述正确的是( )
Z(s)已达到平衡,此时升高温度则气体的密度增大。下列叙述正确的是( )
A.正反应为放热反应,X可能是气态、液态或固态
B.正反应为放热反应,X一定为气态
C.若X为非气态,则正反应为吸热反应
D.若加入少量的Z,该平衡向左移动
查看答案和解析>>
科目:高中化学 来源:2016届河北省张家口市四校高三上学期联考化学试卷(解析版) 题型:选择题
下列反应的产物中,有的有同分异构体,有的没有同分异构体,其中一定不存在同分异构体的反应是
A.甲烷与氯气发生取代反应
B.丙烯与水在催化剂的作用下发生加成反应
C.异戊二烯[CH2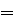 C(CH3)—CH
C(CH3)—CH CH2]与等物质的量的 Br2发生加成反应
CH2]与等物质的量的 Br2发生加成反应
D.2-氯丁烷(CH3CH2CHCICH3)与NaOH乙醇溶液共热发生消去HCl分子的反应
查看答案和解析>>
科目:高中化学 来源:2016届湖南省、修水一中高三上学期联考化学试卷(解析版) 题型:填空题
工业上用某矿渣(主要成分是Cu2O,少量杂质是Al2O3、Fe2O3和SiO2)提取铜的操作流程如下:

已知:Cu2O+2H+==Cu+Cu2++H2O
沉淀物 |
|
|
|
|
开始沉淀pH | 5.4 | 4.0 | 2.2 | 5.8 |
沉淀完成pH | 6.7 | 5.2 | 3.2 | 8.8 |
(1)固体混合物A中的成分是 (填化学式)。
(2)反应I完成后,铁元素的存在形式为 (填离子符号)。
(3)y的数值范围是 。
(4)若电解法获得Cu 64.0g,则原矿渣中Cu2O的质量是 。
a、144.0g b、大于144.0g c、小于144.0g
(5)下列关于用NaClO调节溶液pH的说法正确的是 。
a、加入NaClO可使溶液的pH降低
b、NaClO能调节pH的主要原因是由于发生反应: 消耗H+,从而达到调节pH的目的
消耗H+,从而达到调节pH的目的
c、NaClO能调节pH的主要原因是由于NaClO水【解析】 OH—消耗H+,从而达到调节pH的目的。
OH—消耗H+,从而达到调节pH的目的。
(6)用NaClO调pH,生成沉淀B的同时生成一种具有漂白作用的物质,且该物质与还原产物的物质的量之比为4:1,该反应的离子方程式为 。
查看答案和解析>>
科目:高中化学 来源:2016届天津市等六校高三上学期期中联考化学试卷(解析版) 题型:选择题
若NA代表阿伏加德罗常数,下列说法正确的是( )
A.1 molCl2参加反应转移电子数一定为2 NA
B.将31g的Na2O溶解于1L水中,所得溶液中Na+的物质的量浓度为1 mol/L
C.22.4L的NH3 和16g CH4中所含有的电子数都是10NA
D.20g重水(2H216O)含有的电子数为10NA
查看答案和解析>>
科目:高中化学 来源:2015-2016学年安徽省、泥河中学高二上12月联考化学试卷(解析版) 题型:实验题
50mL0.50mol/L盐酸与50mL0.55mol/LNaOH溶液在下图所示的装置中进行中和反应。通过测定反应过程中所放出的热量可计算中和热。回答下列问题:

(1)从实验装置上看,图中尚缺少的一种玻璃用品是________。
(2)烧杯间填满碎纸条的作用是_____________。
(3)大烧杯上如不盖硬纸板,求得的中和热数值将____________(填“偏大”、“偏小”或“无影响”)。
(4)实验中改用60mL0.50mol/L盐酸与50mL0.55mol/LNaOH溶液进行反应,与上述实验相比较,所放出的热量_____________(填“相等”或“不相等”),但中和热应_________(填“相等”或“不相等”),简述理由_________________________________。
(5)用相同浓度和体积的氨水代替NaOH溶液进行上述实验,测得中和热的数值与57.3kJ/mol相比较会__________;用50mL0.50mol/LNaOH溶液进行上述实验,测得中和热的数值与57.3kJ/mol相比较会__________(均填“偏大”、“偏小”或“无影响”)
查看答案和解析>>
科目:高中化学 来源:2015-2016学年福建省高二上学期期中(文)化学试卷(解析版) 题型:选择题
对于原电池的电极名称,叙述有错误的是:
A. 发生氧化反应的极为负极 B. 正极为电子流入的一极
C. 比较不活泼的金属为负极 D. 电势较高的一极为正极
查看答案和解析>>
科目:高中化学 来源:2015-2016学年河南省高二上学期期中考试化学试卷(解析版) 题型:选择题
已知反应:2SO2(g)+O2(g)  2SO3(g) ΔH<0。某温度下,将2 mol SO2和1 mol O2置于10 L密闭容器中,反应达平衡后,SO2的平衡转化率(α)与体系总压强(p)的关系如图甲所示。则下列说法正确的是( )
2SO3(g) ΔH<0。某温度下,将2 mol SO2和1 mol O2置于10 L密闭容器中,反应达平衡后,SO2的平衡转化率(α)与体系总压强(p)的关系如图甲所示。则下列说法正确的是( )

A.由图甲知,A点SO2的平衡浓度为0.4 mol·L-1
B.由图甲知,B点SO2、O2、SO3的平衡浓度之比为2∶1∶2
C.达平衡后,缩小容器容积,则反应速率变化图象可以用图乙表示
D.压强为0.50 MPa时不同温度下SO2转化率与温度关系如丙图,则T2>T1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com