
| A. | 运输液氯的铁管被腐蚀 | B. | 金属在潮湿空气中更容易腐蚀 | ||
| C. | 铁与酸反应滴加硫酸铜后反应加快 | D. | 含杂质的锌比纯锌与酸反应快 |
分析 A、氯气与铁反应生成三氯化铁;
B、金属在潮湿的空气中容易形成原电池;
C、铁与硫酸铜反应生成铜,铁-铜-酸形成原电池;
D、锌-杂质-酸构成原电池根据原电池,原电池可以加快金属的腐蚀速率.
解答 解:A、氯气与铁反应生成三氯化铁,属于化学腐蚀,不是由于原电池造成的,故A选;
B、金属在潮湿的空气中容易形成原电池而加快腐蚀,是由于原电池造成的,故B不选;
C、铁与硫酸铜反应生成铜,铁-铜-酸形成原电池,化学反应速率加快,是由于原电池造成的,故C不选;
D、锌-杂质-酸构成原电池,反应速率加快,是由于原电池造成的,故D不选;
故选A.
点评 本题考查原电池的工作原理知识,注意原电池原理的应用:加快化学反应速率是重要的一条,难度中等.


 习题精选系列答案
习题精选系列答案科目:高中化学 来源: 题型:选择题
| A. | 离子化合物中一定不含共价键,共价化合物中一定不含离子键 | |
| B. | 含有离子键的化合物一定是离子化合物 | |
| C. | 含有共价键的物质一定是共价化合物 | |
| D. | 分子间作用力越大,分子的热稳定性就越大 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
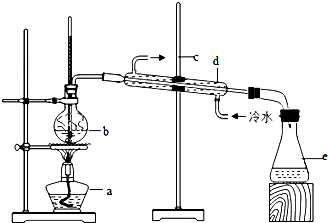
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 | 0 | 10 | 20 | 30 | 40 | 50 |
| 实验1/800 | 1.00 | 0.80 | 0.65 | 0.55 | 0.50 | 0.50 |
| 实验2/800 | 1.00 | 0.70 | 0.50 | 0.50 | 0.50 | 0.50 |
| 实验3/850 | 1.00 | 0.50 | 0.40 | 0.15 | 0.15 | 0.15 |
| A. | 实验2比实验1的反应容器内压强减小 | |
| B. | 实验2比实验l使用了效率更高的催化剂 | |
| C. | 实验1比实验3的平衡常数大 | |
| D. | 实验2和实验3可判断该反应是放热反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 元素 | Al | B | Be | C | Cl | F | Li | Mg | N | Na | O | P | S | Si |
| 电负性 | 1.5 | 2.0 | 1.5 | 2.5 | 3.0 | 4.0 | 1.0 | 1.2 | 3.0 | 0.9 | 3.5 | 2.1 | 2.5 | 1.8 |
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 离子化合物中一定不含共价键,共价化合物中一定不含离子键 | |
| B. | 两种微粒,若核外电子排布完全相同,则其化学性质一定相同 | |
| C. | 碳原子之间可形成碳碳单键、碳碳双键或碳碳叁键 | |
| D. | 分子间作用力越大,分子的热稳定性就越大 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 只有共价键形成的分子一定是共价化合物 | |
| B. | 含有金属阳离子的晶体一定是离子晶体 | |
| C. | 元素的非金属性越强,其单质的活泼性一定越强 | |
| D. | 分子晶体中一定存在分子间作用力,不一定存在共价键 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
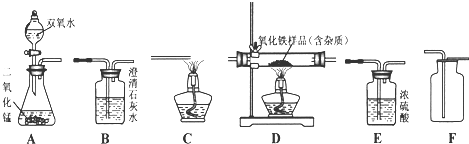
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com