
| A、属于酸类,可能与一些盐发生反应 |
| B、是常见的还原剂,可以被还原成碘单质 |
| C、是电解质,水溶液可以导电 |
| D、属于化合物,受热时可能分解 |


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
| A、达到化学平衡时,5v正(O2)=4v逆(NO) |
| B、达到化学平衡时,3v正(NO)=2v正(H2O) |
| C、当NH3、O2、NO和H2O的浓度相等时,反应一定达到平衡状态 |
| D、达到化学平衡时,若增大容器体积,则正反应速率减小,逆反应速率增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①⑦ | B、②⑦ | C、③④ | D、④⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:
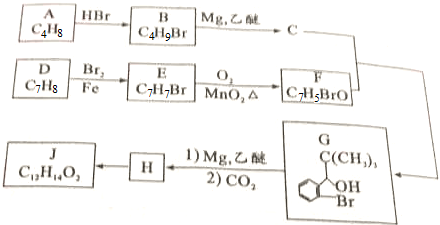
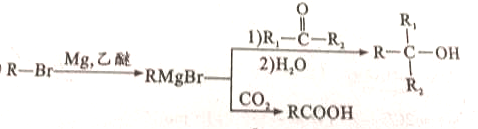
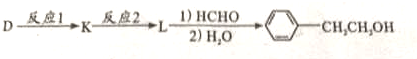
查看答案和解析>>
科目:高中化学 来源: 题型:
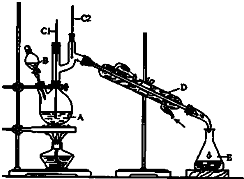 正丁醛是一种化工原料.某实验小组利用如图装置合成正丁醛.
正丁醛是一种化工原料.某实验小组利用如图装置合成正丁醛.| Na2Cr2O7 |
| H2SO4△ |
| 沸点/.c | 密度/(g?cm-3) | 水中溶解性 | |
| 正丁醇 | 111.72 | 0.8109 | 微溶 |
| 正丁醛 | 75.7 | 0.8017 | 微溶 |
查看答案和解析>>
科目:高中化学 来源: 题型:
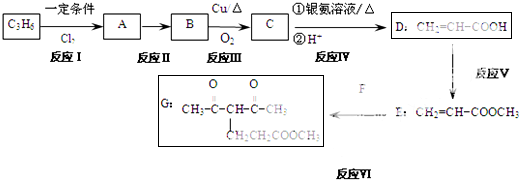
 ,反应Ⅵ属于上面列出的麦克尔反应类型,且F的核磁共振氢谱有两个吸收峰,面积比为3:1,则F的结构简式为
,反应Ⅵ属于上面列出的麦克尔反应类型,且F的核磁共振氢谱有两个吸收峰,面积比为3:1,则F的结构简式为查看答案和解析>>
科目:高中化学 来源: 题型:
| A、一定存在NH4+、Cl-、CO32-、SO42-,可能存在Na+ |
| B、一定存在NH4+、CO32-、SO42-、Na+,一定不存在Ba2+、Cl- |
| C、c(SO42-)=0.2mol?L-1,c(NH4+)>c(SO42-) |
| D、如果溶液中存在NH4+、Cl-、CO32-、SO42-、Na+五种离子,则c(Na+)>0.2mol?L-1 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com