
【题目】下列关于乙醇(C2H5OH)的描述错误的是( )
A.俗称酒精 B.不能与金属钠反应
C.乙醇可用于消毒 D.能与乙酸发生酯化反应
科目:高中化学 来源: 题型:
【题目】以物质的量为中心的相关计算,已知阿伏伽德罗常数为NA.
(1)质量相同的H2、NH3、SO2、O3四种气体中,含有分子数目最少的是___________,在相同温度和相同压强条件下,体积最大的是___________。
(2)73.0g HCl气体中含有_______个分子、________个原子、______个质子、_________个电子,标况下体积约为_______L
(3)23.75 g某+2价金属的氯化物(MCl2)中含有3.01×1023个Cl-,则MCl2的摩尔质量为________, MCl2的相对分子质量为________,M的相对原子质量为________。
(4)将0.5L1mol/L FeCl3溶液加水稀释至1L,所得溶液中氯离子的物质的量浓度是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,向1L0.1mol·L-1NH4Cl溶液中,不断加入固体NaOH后,NH4+与NH3·H2O的变化趋势如图所示(不考虑溶液体积变化和氨的挥发),下列说法正确的是

A.在M点时,n(OH-)-n(H+)=(a-0.05)mol
B.M点溶液中水的电子程度比原溶液的大
C.随着NaOH的加入,c(H+)/c(NH4+)不断增大
D.当n(NaOH)=0.mol时,c(OH-)=c(Cl-)-c(NH3·H2O)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国拥有丰富的海洋资源,海水制盐历史悠久,早在5000年前的仰韶文化时期,先人就利用海水煮盐。为除去粗盐中的Ca2+、Mg2+、Fe3+、SO42- 以及泥沙等杂质,某同学设计了一种制备精盐的实验方案,步骤如下(用于沉淀的试剂稍过量):

(1)第①步操作的名称是__________________,第②步判断BaCl2已过量的方法是_____________。
(2)第④步加入试剂的化学式为_________________________。
(3)第⑤步操作所需玻璃仪器的名称是____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列图示与对应的叙述相符的是
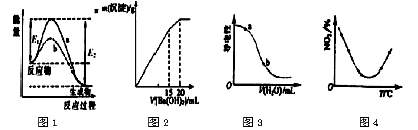
A.图l表示某放热反应在无催化剂(a)和有催化剂(b)时反应的能量变化.且加入催化剂改变反应的焓变
B.图2表示某明矾溶液中加入Ba(OH)2溶液,沉淀的质量与加入Ba(OH)2溶液体积的关系,在加入
20mLBa(OH)2溶液时铝离子恰好沉淀完全
C.图3表示在CH3COOH溶液中加水时溶液的导电性变化,则CH3C00H溶液的pH:a>b
D.图4表示等量NO2在容积相同的恒容密闭容器中.不同温度下分别发生反应:2NO2(g)![]() N2O4(g),相同时间间后测得NO2含量的曲线,则该反应的△H<0
N2O4(g),相同时间间后测得NO2含量的曲线,则该反应的△H<0
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某校化学研究性学习小组的同学探究以铜为电极电解电解质溶液的情况,
第一组同学以铜为电极电解饱和食盐水,探究过程如下:
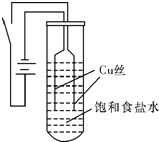
【实验Ⅰ】如图装置,电源接通后,与电池负极相连的铜丝上有大量气泡产生;与电池正极相连的铜丝由粗变细.电解开始30s内,阳极附近出现白色浑浊,然后开始出现橙黄色浑浊,此时测定溶液的pH约为10;随着沉淀量的逐渐增加,橙黄色沉淀慢慢聚集在试管底部,但溶液始终未出现蓝色。
【实验Ⅱ】将实验Ⅰ中试管底部的橙黄色沉淀取出,分装在两支小试管中,沉淀很快转变为砖红色,后续的操作及现象如下:

请回答下列问题:
(1)聚集在试管底部的橙黄色沉淀的化学式为______________.
(2)阳极的电极反应式为______________.
(3)写出实验Ⅱ中①、②的离子方程式:①__________;②__________.
(4)第二组同学将质量相等的铜片和铂片插入硫酸铜溶液中,铜片与电源正极相连铂片与电源负极相连,以电流强度1A通电10min,然后反接电源,以电流强度2A继续通电10min.画出下列表示铜电极、铂电极、电解池中产生气体的质量和电解时间的关系图,其中正确的是( )
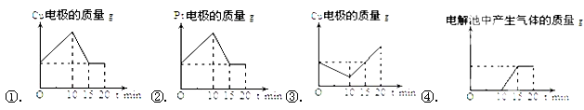
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知lg2=0.3, KSP[Cr(OH)3]=6.4×10-31。某工厂进行污水处理时,要使污水中的Cr3+以Cr(OH)3形式除去,当c(Cr3+)=1×10-5时,可以认为Cr3+沉淀完全,溶液的pH至少为
A.4.4 B.5.6 C.6.7 D.8.4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1).某化学小组利用下图装置进行实验证明氧化性:KMnO4>Cl2>Br2。
限选试剂:KBr溶液、KMnO4、浓盐酸、浓硫酸

装置a、d中盛放的试剂分别是: 、 ;实验中观察到的现象为 ;此实验装置的不足之处是 。
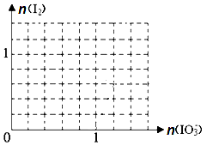
(2)已知:还原性HSO3>I,氧化性IO3> I2,在下图中画出向含3 mol NaHSO3的溶液中逐滴加入KIO3溶液的过程中,析出I2的物质的量与KIO3的物质的量之间关系的曲线。
(3)已知CN-离子、SCN-离子和Cl-离子有相似之处,氰分子(CN)2和硫氰分子(SCN)2的性质与Cl2也有相似之处,且常温常压均为气体,完成下列反应方程式:
①MnO2和HSCN的浓溶液共热的化学方程式: 。
②(CN)2和NaOH溶液反应的离子方程式: 。
(4)已知H2O2是二元弱酸、请写出H2O2与Ca(OH)2溶液反应生成酸式盐的化学式 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com