
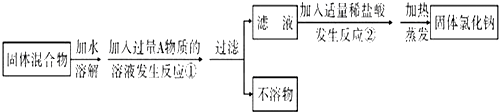
分析 本题中的氯化钠和氯化钙都属于盐,属于除杂质题,除杂质题最少要满足两个条件:①加入的试剂只能与杂质反应,不能与原物质反应②反应时不能加入新的杂质.要除去氯化钠中的少量杂质氯化钙,只要除去钙离子就可以了,氯离子不是杂质.因此可以加入足量A是碳酸钠溶液(俗名纯碱或苏打),生成白色沉淀碳酸钙,从而除去钙离子,得到的沉淀和溶液可以用过滤的方法分开.过量的碳酸钠可以用稀盐酸除去,在每个步骤中都有氯化钠生成,因此氯化钠的质量是增加的.
解答 解:(1)要除去氯化钠中的少量杂质氯化钙,只要除去钙离子就可以了,氯离子不是杂质.因此可以加入足量是碳酸钠溶液,生成白色沉淀碳酸钙,从而除去钙离子.碳酸钠的俗名是纯碱或苏打.故答案为:Na2CO3;纯碱(或苏打);
(2)②的化学方程式是指过量的碳酸钠与稀盐酸的反应,它们互相交换成分生成氯化钠和水和二氧化碳,要注意配平,离子方程式:2H++CO32-═CO2+H20,故答案为:2H++CO32-═CO2+H20;
(3)反应①中加入过量A物质的目的是使氯化钙充分反应;反应②中如果加入盐酸也过量,对所得的氯化钠的纯度无影响,因为盐酸具有挥发性并且是液体.故答案为:使氯化钙完全反应(合理即可);没有.
(4)分离后所得氯化钠的质量与原来氯化钠的质量相比较增多了,原因是每一步除杂质的过程中都生成了氯化钠.故答案为:增大.
点评 本考点属于物质的分离和提纯,题目难度中等,本题利用图式设计出相应的实验步骤,分步骤进行分离,侧重于学生的分析能力、实验能力和评价能力的考查,难度不大,注意把握物质的性质的异同,注意除杂时不能引入新的杂质.


 寒假天地重庆出版社系列答案
寒假天地重庆出版社系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 新制氢氧化铜悬浊液 | B. | 氯化铁溶液 | ||
| C. | 氯化钡溶液 | D. | 酸性高锰酸钾溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
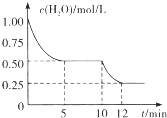 在2L密闭容器中进行反应C(s)+H2O(g)=CO(g)+H2(g )△H>0,测得
在2L密闭容器中进行反应C(s)+H2O(g)=CO(g)+H2(g )△H>0,测得| A. | 0-5 min内,v(H2)=0.05 mol/(L.min) | |
| B. | 5 min时该反应的K值一定小于12 min时的K值 | |
| C. | 10 min时,改变的外界条件可能是减小压强 | |
| D. | 5 min时该反应的v正大于11 min时的v逆 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CsICI2有氧化性,是因为Cs显+3价 | |
| B. | CsICI2有还原性,是因为含有较强还原性的I- | |
| C. | 酸性高锰酸钾溶液中滴加CsICI2溶液,溶液褪色 | |
| D. | 在CsICl2溶液中滴加HNO3,可生成Cl2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 蛋白质“溶液”是一种胶体,向该分散系中加入少量的盐(如硫酸铵)能促进蛋白质的溶解 | |
| B. | 饱和(NH4)2SO4溶液能使蛋白质变性 | |
| C. | 用半透膜可除去蛋白质溶液中的NaCl | |
| D. | 用灼烧的方法检验是毛线还是棉线 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 可用如图所示装置作为实验室制取乙烯的发生装置 | |
| B. | 乙烯与酒精蒸汽按任意物质的量比混合,取VL该气体完全燃烧,相同条件消耗O2体积为3VL | |
| C. | 乙烯、乙醇都能使酸性高锰酸钾溶液褪色,符合通式CnH2n和CnH2n+2O的物质也都能使酸性高锰酸钾溶液褪色 | |
| D. | 甲苯在光照条件和 FeBr3作用下都能与Br2反应,反应产物相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CCl4 和CH2Cl2 | B. | H3O+ 和NH4+ | C. | CaO2 和 CaF2 | D. | Ba(0H)2 和NaOH |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | $\frac{22.4nb}{m{N}_{A}}$L | B. | $\frac{22.4mb}{n{N}_{A}}$ L | C. | $\frac{22.4n{N}_{A}}{mb}$ L | D. | $\frac{nb{N}_{A}}{22.4m}$ L |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com