
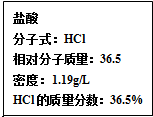
 ��ѧ��������������������Լ���ᷢչ�������еĹ�ϵ��
��ѧ��������������������Լ���ᷢչ�������еĹ�ϵ������ ��1���ٵ���������Ȱ����ƻ������㣻
��ˮ���ԭ����ճ����ʯ��ʯ��������ԭ���Ǵ��ʯ��ʯ��ʯӢ������ԭ���о���ʯ��ʯ��̼��ƣ�
�۶���������������ά��Ҫ�ɷ֣�
��2������ĭ���к���Al�����ݼ��ȣ�������һ�ֺϽ����ݺϽ����ʽ�������Ϣ�жϽ��
������ʳƷ��ȾԴ֮һ������ֻҪ���˿�ǻ�Ӵ��ĺ����������ʾ���Ҫ���Կ��ƣ��ݴ˷������
�۸������Ļ�ѧ���ʽ��з�����
��3������������ɷּ��Ȼ�������жϽ��
������c=$\frac{1000�Ѧ�}{M}$���㣻
��������Һϡ���ɽ�ϣ�����һ�����ʵ���Ũ����Һ���Ʒ������
��� �⣺��1���ٵ���������Ȱ����ƻ������㣬�ʴ�Ϊ��c��
�ڹ�ҵ������ˮ�ࡢ������¯������Ҫ�õ���ԭ����ʯ��ʯ���ʴ�Ϊ��b��
�۹��ά����Ҫ�ɷ��ǣ���ѧ�ɷ�SiO2���ʴ�Ϊ��SiO2��
��2����a��ĭ����һ�ֺϽ����ڻ�����a����
b��������ĭ���ŵ���Ӳ�ȸߣ��ܶ�С����֪����������ɻ�����b��ȷ��
c�����������֪����ĭ��Ӳ�ȸߣ��ܶ�С����ľ�Ļ��ᣬ�ɸ���ˮ�棬���кܴ�ĸ��ԣ��Ҹ��������£���һ�����õĽ������Ϻ����ʲ��ϣ���c��ȷ��
��ѡ��a��
����������ˮ�����˿�ǻ�Ӵ�����Ҫ���ƣ���b��ȷ��
�ʴ�Ϊ��b��
��ͨ�����������Ʒ����ʴ��������Ϊ���ڳ�����������е�����������ѧ��Ӧ�����������һ�����ܵ���������Ĥ���Ӷ���ֹ����һ��������
�ʴ�Ϊ�����ܵ�����Ĥ��
��3����a�Ȼ���ֻ���⡢��Ԫ�أ�������Ԫ�أ���a����
b�������ڻ�����ܹ�������������ӣ��Ȼ������ڴ����ﲻ�ܵ��룬�������ʲ�ͬ����b����
c�Ȼ����ӷ�����c��ȷ��
��ѡ��c��
��Ũ��������ʵ���Ũ��C=$\frac{1000��1.19��36.5%}{36.5}$=11.9g/mol���ʴ�Ϊ��11.9��
��a���ø���������1.19mol/L������480mL��Ӧѡ��500mL����ƿ������ҪŨ�������ΪV����V��11.9mol/L=500mL��1.19mol/L�����V=50.0mL��
b����480mL��Һ��ʵ����û��480mL����ƿ��ʵ��Ӧѡ��500mL����ƿ��
c����ʱ�������ؽ�����ˮע������ƿ�У�ֱ��ƿ�е�Һ��ӽ�����ƿ�Ŀ̶���l��2cm�������ý�ͷ�ιܼ�����ˮ����Һ�İ�Һ��������̶������У�
�ʴ�Ϊ��50.0�� 500����ͷ�ιܣ�
���� ���⿼���������г����Ļ�ѧ֪ʶ���漰������Ⱦ�����������ǽ������ϡ��Ͻ����;�����ʣ�һ�����ʵ���Ũ����Һ�����ƣ���Ŀ�ѶȲ���



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
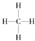 ��һ�����ĸ�����ȼ�չ��̵������仯��ͼ1��ʾ����ͼ�п��Զ���E1��E2����������������÷�Ӧ�ų� ����ų��������ա���������
��һ�����ĸ�����ȼ�չ��̵������仯��ͼ1��ʾ����ͼ�п��Զ���E1��E2����������������÷�Ӧ�ų� ����ų��������ա���������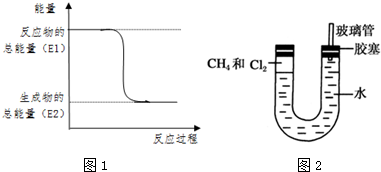
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

 ��
�� $\stackrel{һ������}{��}$
$\stackrel{һ������}{��}$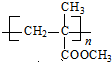 ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| ������� | ��ʼʱ���������ʵ���/mol | ƽ��ʱ��Ӧ�е������仯 | ||
| N2 | H2 | NH3 | ||
| �� | 1 | 3 | 0 | �ų�����a kJ |
| �� | 0 | 0 | 2 | ��������b kJ |
| �� | 2 | 6 | 0 | �ų�����c kJ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
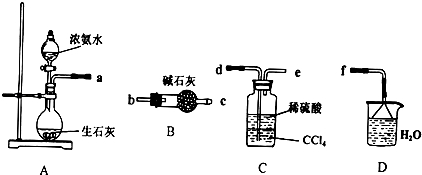 dz��ɫ����������茶���[����Ī���Σ�NH4��2SO4•FeSO4•6H2O]���̷���FeSO4•7H2O�����ȶ��������ڶ���������Ī���ε�һ��ʵ�����Ʒ����£�
dz��ɫ����������茶���[����Ī���Σ�NH4��2SO4•FeSO4•6H2O]���̷���FeSO4•7H2O�����ȶ��������ڶ���������Ī���ε�һ��ʵ�����Ʒ����£��鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
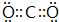 ��
��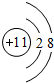 ��D��E����γɵĻ�����ĵ���ʽ
��D��E����γɵĻ�����ĵ���ʽ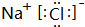 ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | Na+��K+��$S{O_4}^{2-}$��$HC{O_3}^-$ | B�� | Cu2+��K+��$S{O_4}^{2-}$��$N{O_3}^-$ | ||
| C�� | Na+��K+��Cl-��$S{O_4}^{2-}$ | D�� | Fe2+��K+��$N{O_3}^-$��$C{H_3}CO{O^-}$ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ���� | B�� | NH3 | C�� | ���ڵ�K2O | D�� | BaSO4���� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com