
| 沸点 | 溶解性 | ||
| 丙烯酸 | 141℃ | 与水互溶,易溶于有机溶剂 | 有毒 |
| 甲醇 | 65℃ | 与水互溶,易溶于有机溶剂 | 易挥发,有毒 |
| 丙烯酸甲酯 | 80.5℃ | 难溶于水,易溶于有机溶剂 | 易挥发 |
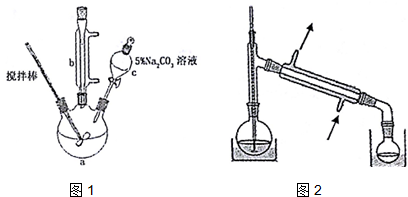
分析 (1)根据装置图可知仪器c的名称;
(2)混合液中有丙烯酸甲酯、丙烯酸、甲醇,丙烯酸能与Na2CO3溶液反应,甲醇能溶于碳酸钠溶液中;
(3)配制100g 5% Na2CO3溶液通常用的玻璃仪器是烧杯、玻璃棒、量筒;
(4)蒸馏装置中温度计的水银球应在蒸馏烧瓶的支管口处,尾接管与锥形瓶接口不能密封,据此答题;
(5)中和过量的KOH,滴到终点时共消耗盐酸20.00mL,即0.5×0.02mol=0.01mol,所以用于水解的KOH的物质的量为0.025mol-0.01mol=0.015mol,所以用于生成CH2=CHCOOCH3的CH2=CHCOOH的质量为0.015mol×72g/mol=1.08g,参加实验的样品为原样品的$\frac{1}{5}$,据此可计算丙烯酸的转化率;
(6)丙烯酸和甲醇都是易燃的所以要防止明火,甲醇易挥发,所以要在通风橱中实验.
解答 解:(1)根据装置图可知仪器c的名称为分液漏斗,故答案为:分液漏斗;
(2)混合液中有丙烯酸甲酯、丙烯酸、甲醇,丙烯酸能与Na2CO3溶液反应,甲醇能溶于碳酸钠溶液中,所以用5%0Na2CO3溶液洗涤的目的是除去混合液中的丙烯酸和甲醇(降低丙烯酸甲酯的溶解度),
故答案为:除去混合液中的丙烯酸和甲醇(降低丙烯酸甲酯的溶解度);
(3)配制100g 5% Na2CO3溶液通常用的玻璃仪器是烧杯、玻璃棒、量筒,
故答案为:烧杯、玻璃棒、量筒;
(4)蒸馏装置中温度计的水银球应在蒸馏烧瓶的支管口处,尾接管与锥形瓶接口不能密封,所以装置图中的错为温度计水银球位置、尾接管与锥形瓶接口密封,
故答案为:温度计水银球位置、尾接管与锥形瓶接口密封;
(5)中和过量的KOH,滴到终点时共消耗盐酸20.00mL,即0.5×0.02mol=0.01mol,所以用于水解的KOH的物质的量为0.025mol-0.01mol=0.015mol,所以用于生成CH2=CHCOOCH3的CH2=CHCOOH的质量为0.015mol×72g/mol=1.08g,参加实验的样品为原样品的$\frac{1}{5}$,所以丙烯酸的转化率为$\frac{1.08}{10×\frac{1}{5}}$×100%=54.0%,
故答案为:54.0%;
(6)丙烯酸和甲醇都是易燃的所以要防止明火,甲醇易挥发,所以要在通风橱中实验,所以本实验中需要采取的安全防护措施为通风橱中实验、防止明火,
故答案为:通风橱中实验、防止明火.
点评 本题考查有机物的合成,侧重对化学实验的考查,涉及对装置的理解、物质的分离提纯、对实验条件的控制、对数据的分析处理等,难度中等,需要学生基本知识的基础与灵活运用能力.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
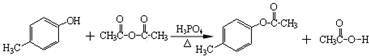
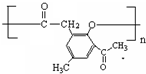
 +(2n-1)H2O.
+(2n-1)H2O. .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 .
. .
. .
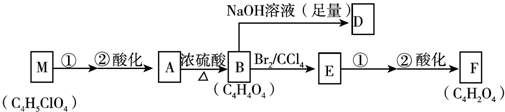
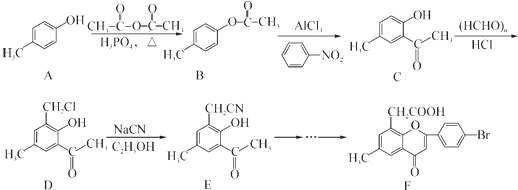
.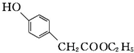 )是一种重要的医药中间体.写出以A和乙醇为主要原料制备对羟基苯乙酸乙酯的合成路线流程图(无机试剂任选).合成路线流程图示例如下:
)是一种重要的医药中间体.写出以A和乙醇为主要原料制备对羟基苯乙酸乙酯的合成路线流程图(无机试剂任选).合成路线流程图示例如下: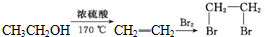
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常温下,0.1mol/LNa2S溶液中存在:c(OH-)=c(H+)+c(HS-)+c(H2S) | |
| B. | 0.1mol/LNaHCO3溶液与0.1mol/LNaOH溶液等体积混合,所得溶液中:C(Na+)>c(CO32-)>c(HCO3- )>c(OH-)>c(H+) | |
| C. | pH相同的①CH3 COONa②NaHCO3③NaClO三种溶液的c(Na+):①>②>③ | |
| D. | 向0.1mol•L-1的氨水中加入少量硫酸铵固体,则溶液中$\frac{c(O{H}^{-})}{c(N{H}_{3}•{H}_{2}O)}$增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
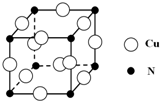 硼和氮元素在化学中有很重要的地位,回答下列问题:
硼和氮元素在化学中有很重要的地位,回答下列问题: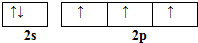 .预计于2017年发射的“嫦娥五号”探测器采用的长征5号运载火箭燃料为偏二甲肼[(CH3)2NNH2].(CH3)2NNH2中N原子的杂化方式为sp3.
.预计于2017年发射的“嫦娥五号”探测器采用的长征5号运载火箭燃料为偏二甲肼[(CH3)2NNH2].(CH3)2NNH2中N原子的杂化方式为sp3.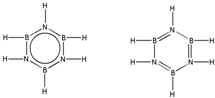 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | HCO3-+H2O?H3O-+CO32- | B. | CO32-+H2O?HCO3-+OH- | ||
| C. | NH3+H2O?NH3•H2O | D. | HCO3-+OH-═H2O+CO32- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 物质 | 杂质 | 试剂 | 提纯方法 |
| A | BaSO4 | BaCO3 | 水 | 溶解、过滤、洗涤 |
| B | CO2 | SO2 | 饱和 Na2CO3 溶液 | 洗气 |
| C | 乙烷 | 乙烯 | 酸性 KMnO4 溶液 | 洗气 |
| D | 蛋白质 | 葡萄糖 | 浓 (NH4)2SO4 溶液 | 盐析、过滤、洗涤 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com