
下列说法正确的是( )
A.CS2是极性键构成的极性分子
B.SO2与CO2为等电子体
C.金属晶体的六方最密堆积和面心立方最密堆积的方式空间利用率最高
D.1molNaHSO4熔融态时有3mol离子
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源:2016-2017学年广西省桂林市高一下学期开学考试化学试卷(解析版) 题型:选择题
向含有FeBr2、FeI2的溶液中通入一定量的氯气后,再向溶液中滴加KSCN溶液,溶液变为红色,则下列叙述不正确的是
A. 通入氯气之后原溶液中的Fe2+全部被氧化
B. 通入氯气后的溶液中一定不存在I﹣
C. 原溶液中的Br﹣可能被氧化
D. 若取少量所得溶液,再加入CCl4溶液充分振荡,静置、分液,下层溶液可能呈紫红色
查看答案和解析>>
科目:高中化学 来源:2017届河北省石家庄市高三下学期模拟联考理科综合化学试卷(解析版) 题型:简答题
碱式碳酸铜(Cu2(OH)2CO3)是名贵的矿物宝石孔雀石的主要成分,应用广泛,如在无机工业中用于制造各种铜化合物,有机工业中用作有机合成催化剂等等,某化学小组为了探究碱式碳酸铜生成条件对其产率的影响,设计了如下实验:
设计原理:取一定体积的碳酸钠溶液(0.5mol/L)于100mL烧杯中,进行加热,恒温后将硫酸铜溶液(5.00mL. 0.5mol/L)在不断搅拌下以一定速度逐滴加入到上述碳酸钠溶液中,反应达平衡后,静止,减压过滤,洗涤,烘干,即得到最终产品,同时有气体放出。
(1)反应原理为:________________。
(2)探究反应原料用量比对反应产物的影响。
该化学小组根据所提供试剂设汁两个实验来说明反应原料用量对产品的影响
提供试剂:0.5mol/LNa2CO3溶液、0.5mol/LCuSO4溶液。
①请填写下表的空白处:
① | ② | ③ | ④ | |
硫酸铜溶液体积/mL | 2.0 | 2.0 | 2.0 | 2.0 |
碳酸钠溶液体积/mL | 1.6 | 2.0 | 2.8 | |
Na2CO3/CuSO4mol/比) | 0.8 | 1 | 1.4 |
②通过实验画图可知:当比值为______,碱式碳酸铜产量最好。
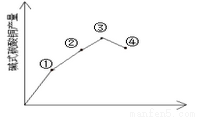
(3)反应温度对产率的影响
在三支试管中各加入2.0mL0.5 mol/LCuSO4溶液另取四支试管各加入由上述实验得到的合适用量的0.5 mol /L Na2CO3溶液。从这两列试管中各取一支将它们分別置于室温、30℃、50℃、100℃的环境中数分钟后将CuSO4溶液倒入Na2CO3溶液中振荡并观察现象,发现:沉淀颜色分别为蓝色沉淀,绿色沉淀、深绿色沉淀,绿色中带有黑色沉淀,实验结果也如上图所示,请思考,为什么温度过髙产率反而下降_______,该实验加热方式为____________。
(4)分析所制得的碱式碳酸铜的质量分数。
将已准确称量的0.5g试样样品放入300mL的锥形瓶中,加入5mL醋酸,适热使其溶解,再用l00mL水将其稀释。加入2.5gKI振荡混合,经过5分钟后,加入数滴淀粉溶液,用0.1mol/L的硫代硫酸钠溶液进行滴定。当_______时即达滴定的终点。
反应的原理:2Cu2++4I- =2CuI+I2,I2+2S2O32-=2I-+S4O62-
用0.lmol/L硫代硫酸钠40 mL,那么试样中铜的质量百分率为________。该溶液的滴定度为_______。(毎毫升标准溶液相当于被测物质的质量,单位是g/mL或mg/mL)(保留三位有效数字)。
查看答案和解析>>
科目:高中化学 来源:2017届福建省厦门市高三下学期第一次质量检测理综化学试卷(解析版) 题型:选择题
己知 ,下列说法错误的是
,下列说法错误的是
A. 该反应属于加成反应 B. 异丙苯的一氯代物共有6种
C. 可用溴水鉴别异丙烯苯和异丙苯 D. 异丙苯是苯的同系物
查看答案和解析>>
科目:高中化学 来源:2016-2017学年四川省成都简阳市高二上学期期末检测化学试卷(解析版) 题型:选择题
在10L恒容密闭容器中充入X(g)和Y(g),发生反应X(g)+Y(g) M(g)+N(g)
M(g)+N(g)
实验编号 | 温度/℃ | 起始时物质的量/mol | 平衡时物质的量/mol | |
n(X) | n(Y) | n(M) | ||
① | 700 | 0.40 | 0.10 | 0.090 |
② | 800 | 0.10 | 0.40 | 0.080 |
③ | 800 | 0.20 | 0.20 | a |
④ | 800 | 0.10 | 0.10 | b |
下列说法正确的是 ( )
A. 实验①中,若5min时测得n(M)=0.050mol,则0至5min时间内,用N表示的平均反应速率υ(N)=1.0×10-2mol/(L·min)
B. 实验②中,该反应的平衡常数K=2.0
C. 实验③中,达到平衡时,X的转化率为50%
D. 实验④中,达到平衡时,b<0.05
查看答案和解析>>
科目:高中化学 来源:2016-2017学年四川省成都简阳市高二上学期期末检测化学试卷(解析版) 题型:选择题
某反应过程能量变化如图所示,下列说法正确的是 ( )
A.反应过程a有催化剂参与
B.该反应为吸热反应,热效应等于∆H
C.改变催化剂,可改变该反应的活化能
D.有催化剂的条件下,反应的活化能等于E1+E2
查看答案和解析>>
科目:高中化学 来源:2016-2017学年四川省成都简阳市高二上学期期末检测化学试卷(解析版) 题型:选择题
钛号称“崛起的第三金属”,被广泛应用于军事、医学等领域。已知钛有48Ti、49 Ti、50Ti等同位素,下列关于金属钛的叙述中不正确的是( )
A. 钛元素在周期表中处于第四周期ⅡB族 B. 上述钛原子中,中子数不可能为22
C. 钛原子的外围电子层排布为3d24s2 D. 钛元素位于元素周期表的d区,是过渡元素
查看答案和解析>>
科目:高中化学 来源:山东省2016-2017学年高一3月月考化学试卷 题型:选择题
13C-NMR(核磁共振)可用于含碳化合物的结构分析,15N-NMR可用于测定蛋白质、核酸等生物大分子的空间结构,下面有关13C、15N叙述正确的是( )
A. 13C与15N具有相同的中子数 B. 13C与C60是同一种物质
C. 15N与14N互为同位素 D. 15N的核外电子数与中子数相同
查看答案和解析>>
科目:高中化学 来源:2017届江苏省南京市、盐城市高三第二次模拟考试化学试卷(解析版) 题型:实验题
硫酸锌可用于制造锌钡白、印染媒染剂等。用锌白矿(主要成分为ZnO,还含有Fe2O3、CuO、SiO2等杂成) 制备ZnSO4 ·7H2O的流程如下。
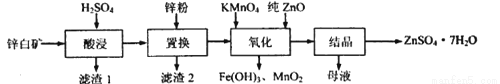
相关金属离了生成氢氧化物沉淀的pH (开始沉淀的pH按金属离子浓度为1.0mol·L-1计算)如下表:
金属离子 | 开始沉淀的pH | 沉淀完全的pH |
Fe3+ | 1.1 | 3.2 |
Fe2+ | 5.8 | 8.8 |
Zn2+ | 6.4 | 8.0 |
(1)“滤渣1”的主要成分为_________(填化学式)。“酸浸”过程中,提高锌元素浸出率的措施有:适当提高酸的浓度、______________(填一种)。
(2)“置换”过程中,加入适量的锌粉,除与溶液中的Fe3+,H+反应外,另一主要反应的化学方程式为__________________________。
(3)“氧化”一步中,发生反应的离子方程式为_______________________。溶液pH控制在[3.2,6.4)之间的目的是________________。
(4)“母液”中含有的盐类物质有_________ (填化学式)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com