
| A. | 弱酸性溶液中:Na+、Mg2+、HSO3-、ClO- | |
| B. | 0.1mol•L-1氨水溶液中:K+、Na+、NO3-、AlO2- | |
| C. | 与Al反应能放出H2的溶液中:Fe3+、K+、NO3-、SO42- | |
| D. | 0.1 mol•L-1Fe(NO3)3溶液中:H+、Al3+、SO32-、Cl- |
分析 A.离子之间发生氧化还原反应;
B..1mol•L-1氨水溶液呈碱性;
C.与Al反应能放出H2的溶液可能呈酸性或碱性;
D.Fe(NO3)3溶液具有氧化性.
解答 解:A.HSO3-、ClO-离子之间发生氧化还原反应,不能大量共存,故A错误;
B..1mol•L-1氨水溶液呈碱性,碱性条件下离子之间不发生任何反应,可大量共存,故B正确;
C.与Al反应能放出H2的溶液可能呈酸性或碱性,碱性条件下Fe3+不能大量共存,酸性条件下因存在NO3-,不生成氢气,故C错误;
D.Fe(NO3)3溶液具有氧化性,酸性条件下SO32-不能大量共存,故D错误.
故选B.
点评 本题考查离子的共存,为高频考点,把握习题中的信息及常见离子之间的反应为解答的关键,侧重复分解反应的离子共存考查,题目难度不大.


 星级口算天天练系列答案
星级口算天天练系列答案 芒果教辅达标测试卷系列答案
芒果教辅达标测试卷系列答案科目:高中化学 来源: 题型:选择题
| A. | α1=α2<α3=α4 | B. | α1=α3<α2=α4 | C. | α1>α2>α3>α4 | D. | α1=α4>α2=α3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 该溶液中SO42-的浓度为0.1mol•L-1 | |
| B. | 该溶液中SO42-的物质的量为0.1mol | |
| C. | 与16.0gCuSO4溶于1L水中所得溶液的浓度相等 | |
| D. | 与16.0gCuSO4•5H2O溶于水中,然后稀释至1L所得溶液的浓度相等 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Fe2+、H+、SO42-、MnO4- | B. | Al3+、Na+、Cl-、AlO2- | ||
| C. | Ba2+、Na+、HCO3-、Cl- | D. | Fe3+、Mg2+、SCN-、Cl- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 钠保存在煤油中 | |
| B. | 保存碱性溶液的试剂瓶的瓶塞要用橡胶塞 | |
| C. | 硝酸保存到棕色的试剂瓶中,并放置在冷暗处 | |
| D. | 氢氟酸保存到玻璃试剂瓶中 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 大气中PM2.5比表面积大,吸附力强,能吸附许多有毒、有害物质 | |
| B. | 氯气分别和氢氧化钠溶液、石灰乳反应得到的所有含氯化合物都具有漂白性 | |
| C. | 石墨烯是一种由单层碳原子构成的新纳米材料,具有导电性 | |
| D. | 刚玉、红宝石主要成分是氧化铝,陶瓷、分子筛主要成分是硅酸盐 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 若a为锌块,铁片腐蚀加快 | |
| B. | 若a为石墨,铁片被保护 | |
| C. | 若a为石墨,a上电极反应为O2+2H2O+4e-=4OH- | |
| D. | 若a为锌块,铁片上电极反应为2H++2e-=H2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
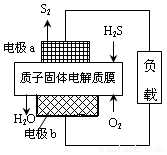 工业废气H2S经资源化利用后可回收能量并得到单质硫.反应原理为:2H2S(g)+O2(g)=S2(s)+2H2O(l)△H=-632kJ•mol-1.H2S燃料电池的工作原理如图所示.下列说法不正确的是( )
工业废气H2S经资源化利用后可回收能量并得到单质硫.反应原理为:2H2S(g)+O2(g)=S2(s)+2H2O(l)△H=-632kJ•mol-1.H2S燃料电池的工作原理如图所示.下列说法不正确的是( )| A. | 电极a为电池的正极 | |
| B. | 电极b上发生的电极反应为O2+4H++4e-=2H2O | |
| C. | 若电路中通过2mol电子,则电池内部释放632kJ热能 | |
| D. | 若有17gH2S参与反应,则会有1molH+经质子膜进入正极区 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com