
分析 (1)A元素原子核外M层电子数是L层电子数的一半,则A原子有3个电子层,最外层电子数为4,为Si元素;
(2)B元素原子的最外层电子数是次外层电子数的1.5倍,最外层电子数不超过8,故该原子只能有2个电子层,最外层电子数为3,为硼元素;
(3)C元素的单质在常温下可与水剧烈反应,产生的气体能使带火星的木条复燃,则C为F元素;
(4)D元素的次外层电子数是最外层电子数的$\frac{1}{4}$,最外层电子数不超过8,则次外层为K层,最外层电子数为8,为Ne元素.
解答 解:(1)A元素原子核外M层电子数是L层电子数的一半,则A原子有3个电子层,最外层电子数为4,核外电子排布式为1s22s22p63s23p2,为硅元素,
故答案为:硅,1s22s22p63s23p2;
(2)B元素原子的最外层电子数是次外层电子数的1.5倍,最外层电子数不超过8,故该原子只能有2个电子层,最外层电子数为3,核外电子排布式为1s22s22p1,为硼元素,
故答案为:硼,1s22s22p1;
(3)C元素的单质在常温下可与水剧烈反应,产生的气体能使带火星的木条复燃,则C为氟元素,核外电子排布式为:1s22s22p5,
故答案为:氟,1s22s22p5;
(4)D元素的次外层电子数是最外层电子数的$\frac{1}{4}$,最外层电子数不超过8,则次外层为K层,最外层电子数为8,核外电子排布式为1s22s22p6,为氖元素,
故答案为:氖,1s22s22p6.
点评 本题考查核外电子排布、结构与位置关系,关键是对核外电子排布规律的理解掌握,有利于基础知识的巩固.


 七彩题卡口算应用一点通系列答案
七彩题卡口算应用一点通系列答案科目:高中化学 来源: 题型:选择题
| A. | 二氧化硫的接触氧化在合成塔中发生 | |
| B. | 吸收塔得到的硫酸浓度为98% | |
| C. | 煅烧含硫48%的黄铁矿时,若FeS2损失了2%,则S损失4% | |
| D. | 接触室中适宜条件是V2O5作催化剂、高温、常压 | |
| E. | 接触室中采取高温是为了提高催化剂的活性和提高SO2的转化率 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 分子式为C5H10O2的酯类 | B. | 分子式为C5H10的烯烃 | ||
| C. | 分子式为C5H12O的醇类 | D. | 分子式为C5H12的所有化合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
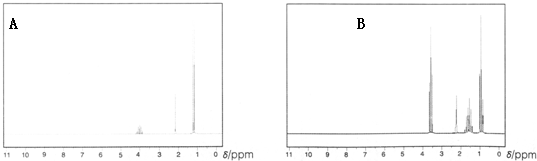
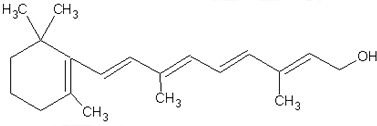
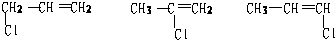 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 某同学利用下列实验装置图探究铜与稀硝酸反应的还原产物并进行喷泉实验(假设药品足量),请回答下列问题:
某同学利用下列实验装置图探究铜与稀硝酸反应的还原产物并进行喷泉实验(假设药品足量),请回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原子半径:X<Y | |
| B. | 第一电离能:X>Y | |
| C. | 气态氢化物的稳定性:HmY小于HnY | |
| D. | X与Y形成化合物时,一般显负价,Y显正价 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 石灰石与盐酸反应:CO32ˉ+2H+═H2O+CO2↑ | |
| B. | 稀硫酸溶液与氢氧化钡溶液反应:Ba2++SO42-═BaSO4↓ | |
| C. | 铁粉与稀盐酸反应:2Fe+6H+═2Fe3++3H2↑ | |
| D. | 稀硫酸与氢氧化钠溶液反应:H++OHˉ═H2O |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com