
【题目】下列物质中含有共价键的离子化合物是
A. Ba(OH)2B. H2SO4C. HClD. MgCl2
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】某有机化合物结构简式如图,下列有关它的性质的叙述中,正确的是( ) 
A.有弱酸性,与Na2CO3、NaHCO3溶液均能反应
B.在一定条件下,1 mol该物质最多能与3 mol NaOH完全反应
C.在一定条件下,该物质可以发生取代、加成、水解、消去反应
D.该有机物分子中所有碳原子可能共平面
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学在文物的保护和鉴定方面发挥着重要的作用.已知氨水能够清洗壁画表面的污垢,醋酸可以固色.某文物保护单位现用500mL容量瓶配制0.1molL﹣1的氨水,以下操作正确的是( )
A.将标准状况下1.12 L NH3溶于500 mL水中
B.将标准状况下1.12 L NH3溶于水配成500 mL溶液
C.取1 molL﹣1的氨水50 mL,加入500 mL水中
D.取1 molL﹣1的氨水100 mL,配成1 000 mL溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一种锌/铁液流贮能电池结构如图所示.下列说法正确的是( ) 
A.放电时,Na+从中间室进入负极室
B.充电时,Cl﹣从阳极室进入中间室
C.放电时,负极的电极反应为Zn+4OH﹣﹣2e﹣=Zn(OH)42﹣
D.充电时,阳极的电极反应为Fe3++e﹣=Fe2+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于化学电源的叙述,错误的是
A. 化学电源是根据原电池的工作原理设计的
B. 在干电池中,碳棒作正极,并不参与化学反应
C. 镍镉电池不能随意丢弃的主要原因是镍、镉的资源有限,价格昂贵
D. 铅蓄电池是一种二次电池,其中铅作电池的负极材料
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据问题填空:
(1)I.20mL0.1mol/LBaCl2溶液中Cl﹣的物质的量浓度为 , Ba2+的物质的量为 .
(2)II.把5.1g镁铝合金的粉末放入过量的盐酸中,得到5.6LH2(标准状况下). ①合金中镁的物质的量 .
②写出该合金溶于足量NaOH溶液的化学方程式 . 同时产生H2的体积(标准状况下)为 .
(3)III.在一定质量的AlCl3和MgCl2混合溶液中逐渐滴入一定溶质质量分数的NaOH溶液,生成沉淀的物质的量与加入NaOH的物质的量的关系如图所示,则: 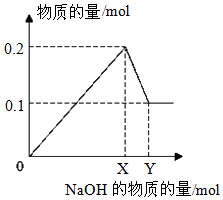
①生成Mg(OH)2的质量为;
②X=;Y= .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一氯甲烷,也叫甲基氯,常温下是无色气体,密度为0.9159g/cm3 , 熔点为﹣97.73℃,沸点为﹣24.2℃,18℃时在水中的溶解度为280mL/mL水,与乙醚、丙酮或苯互溶,能溶于乙醇.在实验室里可用下图装置制造一氯甲烷:制备装置的分液漏斗和烧瓶中分别盛有甲醇和浓盐酸. 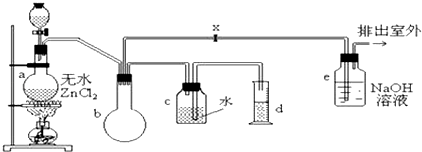
试填写下列空白:
(1)制备一氯甲烷的化学方程式 , 其反应类型属于反应;
(2)装置b的作用是;
(3)已知卤代烃能发生碱性水解,转化为醇.装置e中可能发生的反应方程为; .
(4)检验气体产物CH3Cl的方法是:在e的逸出口点燃CH3Cl气体,火焰呈蓝绿色(燃烧产物中含氯产物只有HCl).则CH3Cl燃烧的化学方程式是;
(5)实验中实际按甲醇和浓盐酸1:2(物质量之比)进行反应的理由是;
(6)某学生在关闭活塞x的情况下做此实验时发现,收集到一定体积的气体产物所消耗的甲醇浓盐酸的混和液的量比正常情况下多(装置的气密性没有问题),其原因是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA表示阿伏伽德罗常数的值,下列叙述正确的是( )
A.常温常压下,11.2 L CO和CO2混合气体中含有的碳原子数目为0.5NA
B.标准状况下,7.1 g氯气与足量氢氧化钠溶液反应转移的电子数为0.2NA
C.常温常压下,4.6 g乙醇中含有的极性共价键数目为0.8NA
D.在1 L 1.0 molL﹣1碳酸钠溶液中,阴离子总数大于NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各物质中,化学键类型完全相同的是( )
A.Na2O2和NaOH B.CH3COONa和NaOH
C.CCl4和H2O D.CO2和H2O2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com