
| A. | 3 | B. | 4 | C. | 5 | D. | 6 |
分析 根据溶液中电荷守恒c(NH4+)+c (Na+)+c(H+)=c (NO3-)+2×c (SO42-)+c(OH-)计算酸雨中氢离子浓度,再根据pH的计算公式计算溶液的pH.
解答 解:溶液中阴阳离子所带电荷总数相等,设氢离子浓度为c,则:c(NH4+)+c (Na+)+c(H+)=c (NO3-)+2×c (SO42-)+c(OH-),由于氢氧根离子浓度较小,可忽略不计,则:2×10-5mol/L+5.0×10-6 mol/L+c(H+)=2.0×10-4 mol/L+2×4.0×10-4 mol/L,
解得:c(H+)=10-3mol/L-2.5×10-5mol/L≈10-3mol/L,
该酸雨的pH=3,
故选A.
点评 本题考查了溶液的pH的简单计算,题目难度不大,明确溶液中阴阳离子所带电荷相等是解本题的关键,注意掌握溶液pH的概念及计算方法.


 每日10分钟口算心算速算天天练系列答案
每日10分钟口算心算速算天天练系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原子半径:As>C1>P | B. | 热稳定性:HC1>AsH3>HBr | ||
| C. | 还原性:As3->S2->C1- | D. | 酸性:H3AsO4>H2SO4>H3PO4 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
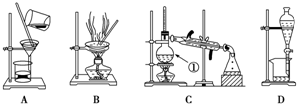
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 上述钛原子中,中子数不可能为22 | |
| B. | 钛元素在周期表中处于第四周期ⅡB族 | |
| C. | 钛原子的外围电子层排布为3d24s2 | |
| D. | 钛元素位于元素周期表的d区,是过渡元素 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 弱酸 | CH3COOH | HCN | H2CO3 |
| 电离平衡常数Ka | 1.8×10-5 | 4.9×10-10 | Ka1=4.3×10-7; Ka2=5.6×10-11 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com