
| A. | CH3CH3+Cl2 $\stackrel{光照}{→}$CH3CH2Cl+HCl | |
| B. | CH2═CH2+HBr→CH3CH2Br | |
| C. | 2CH3CH2OH+O2$→_{△}^{Cu}$2CH3CHO+2H2O | |
| D. | CH3COOH+CH3CH2OH$?_{△}^{浓硫酸}$H3COOCH2CH3+H2O |
分析 A.氯气与乙烷发生取代反应;
B.碳碳双键断裂,生成单键的反应为加成反应;
C.有机反应中加氧、去氢的反应为氧化反应;
D.乙酸与乙醇发生酯化反应生成乙酸乙酯和水,酯化反应属于取代反应;
解答 解:A.在光照条件下,氯气与乙烷发生取代反应,生成CH3CH2Cl和HCl,属于取代反应,故A错误;
B.碳碳双键断裂,生成单键的反应为加成反应,则CH2═CH2+HBr→CH3CH2Br属于加成反应,故B正确;
C.有机反应中加氧、去氢的反应为氧化反应,则2CH3CH2OH+O2$→_{△}^{Cu}$2CH3CHO+2H2O属于氧化反应,故C错误;
D.酯化反应属于取代反应,则CH3COOH+CH3CH2OH$?_{△}^{浓硫酸}$H3COOCH2CH3+H2O属于取代反应,故D错误.
故选B.
点评 本题考查了取代反应、加成反应的判断,难度不大,正确理解概念是解本题的关键.


 亮点激活精编提优100分大试卷系列答案
亮点激活精编提优100分大试卷系列答案科目:高中化学 来源: 题型:解答题
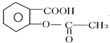 具有的官能团有酯基和羧基(写名称).用阿司匹林和氢氧化钠中和制得可溶性阿司匹林,该反应的化学方程式为C6H5OOCCH3COOH+H2O→CH3COOH+C6H5OHCOOH.
具有的官能团有酯基和羧基(写名称).用阿司匹林和氢氧化钠中和制得可溶性阿司匹林,该反应的化学方程式为C6H5OOCCH3COOH+H2O→CH3COOH+C6H5OHCOOH.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 不慎将酸溅到眼中,应立即用水冲洗,边洗边眨眼睛 | |
| B. | 不慎将浓碱溶液沾到皮肤上,要立即用大量水冲洗,然后涂上硼酸 | |
| C. | 酒精灯着火时可用湿布扑灭 | |
| D. | 蒸馏时,温度计水银球应浸没在液体中 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 工业上常使用过量的空气,目的是为了使SO2的转化率达100% | |
| B. | 工业上选用V2O5作该反应的催化剂,目的是为了加快化学反应速率 | |
| C. | 工业上常选用常压,原因是增大压强不能改变该反应的化学反应速率 | |
| D. | 升高温度可以加快反应速率,所以在工业生产中该反应温度越高越好 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题



查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com