

 =1012��
=1012�� Al(OH)3+3H+�� ��AlO2-+H++H2O=Al(OH)3�� ��Al2O3+2OH-=2AlO2-+H2O
Al(OH)3+3H+�� ��AlO2-+H++H2O=Al(OH)3�� ��Al2O3+2OH-=2AlO2-+H2O �� ��2Cl-+2H2O
�� ��2Cl-+2H2O H2��+Cl2��+2OH-�� ��O2+4e-+2H2O=4OH-
H2��+Cl2��+2OH-�� ��O2+4e-+2H2O=4OH- 4NO+6H2O ��N2(g)+O2(g)=2NO(g) ��H="+180" kJ/mol
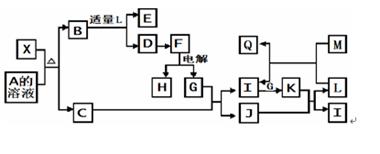
4NO+6H2O ��N2(g)+O2(g)=2NO(g) ��H="+180" kJ/mol Al(OH)3+3H+ ��C��D AlO2-+H++H2O=Al(OH)3����E��C Al2O3+2OH-=2AlO2-+H2O
Al(OH)3+3H+ ��C��D AlO2-+H++H2O=Al(OH)3����E��C Al2O3+2OH-=2AlO2-+H2O .�ڵ�ⱥ��NaCl��ˮ��Һ�����ӷ���ʽΪ2Cl-+2H2O
.�ڵ�ⱥ��NaCl��ˮ��Һ�����ӷ���ʽΪ2Cl-+2H2O H2��+Cl2��+2OH-������������NaCl��Һ����������������ʴ�������ĵ缫��ӦΪO2+4e-+2H2O=4OH-�������ĵ缫ʽΪFe-2e-=Fe2+.
H2��+Cl2��+2OH-������������NaCl��Һ����������������ʴ�������ĵ缫��ӦΪO2+4e-+2H2O=4OH-�������ĵ缫ʽΪFe-2e-=Fe2+. =1012����A��N2��B��NH3��C��NO��D��NO2��E��HNO3����B��C�Ļ�ѧ����ʽΪ��4NH3+5O2
=1012����A��N2��B��NH3��C��NO��D��NO2��E��HNO3����B��C�Ļ�ѧ����ʽΪ��4NH3+5O2 4NO+6H2O��A��C�ķ�Ӧ���Ȼ�ѧ����Ϊ��N2(g)+O2(g)=2NO(g) ��H="+180" kJ/mol��
4NO+6H2O��A��C�ķ�Ӧ���Ȼ�ѧ����Ϊ��N2(g)+O2(g)=2NO(g) ��H="+180" kJ/mol��


| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��6��8 | B��16��8 | C�� 12��9 | D�� 11��6 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A������Ϊͬλ�� | B������Ϊͬ�������� |
| C����������ͬһ�ֺ��� | D���������ڲ�ͬ��Ԫ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��1H��2H�Dz�ͬ�ĺ��أ����ǵ���������ͬ |
| B��14C��14N�����������ȣ����ǵ���������� |
| C�� 6Li��7Li����������ȣ�������Ҳ��� |
| D��13C��14C����ͬһ��Ԫ�أ����ǵ���������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������

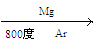 Ti
Ti�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
A����ԭ�ӵĺ�������Ų�ʽΪ�� |
| B����Ԫ�����ڱ��Ԫ�����ڵ����������ں�������ܼ��� |
| C����Ԫ�����ڱ������Ԫ�����ڵ�����������ԭ�Ӻ�������� |
| D�����������������͵���������ȣ����Dz�������һ�����Ӻ�һ�ַ��� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com