
 ;
; .
. 分析 甲、乙、丙、丁是四种短周期元素,甲原子中K层与M层电子数相等,则甲的原子核外电子分三层排布,最外层电子数为2,所以甲为Mg;乙是原子的半径最小的元素,则乙为H元素;丙原子获得一个电子后核外电子排布和Ar原子结构相同,则丙的核外有17个电子,即丙为Cl元素;丁和H两元素可以形成原子个数比为1:1和1:2两种化合物,则丁为O元素;再结合元素周期律解答.
解答 解:甲、乙、丙、丁是四种短周期元素,甲原子中K层与M层电子数相等,则甲的原子核外电子分三层排布,最外层电子数为2,所以甲为Mg;乙是原子的半径最小的元素,则乙为H元素;丙原子获得一个电子后核外电子排布和Ar原子结构相同,则丙的核外有17个电子,即丙为Cl元素;丁和H两元素可以形成原子个数比为1:1和1:2两种化合物,则丁为O元素;
(1)由分析可知,甲为Mg元素,Mg与Cl形成的化合物为氯化镁,MgCl2属于离子化合物,Mg最外层两个电子被两个Cl原子得到,用电子式表示形成过程为: ,
,
故答案为:Mg; ;
;
(2)乙为H元素,在周期表中位于第一周期第IA族;
故答案为:H;第一周期第IA族;
(3)丙为Cl元素,其名称为氯,氯元素的最高价氧化物的水化物为高氯酸,化学式为:HClO4;
故答案为:氯;HClO4;
(4)丁为氧元素,O与H元素形成的具有强氧化性的物质为过氧化氢,过氧化氢为共价化合物,分子中存在两个氧氢键和一个O-O键,双氧水的电子式为: ,
,
故答案为:氧; .
.
点评 本题考查原子结构和元素性质,题目难度中等,根据原子结构确定元素是解题的关键,需要学生熟练掌握核外电子排布规律,有利于基础知识的巩固.


 怎样学好牛津英语系列答案
怎样学好牛津英语系列答案科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 某课外兴趣小组欲测定某NaOH溶液的浓度,其操作步骤如下:
某课外兴趣小组欲测定某NaOH溶液的浓度,其操作步骤如下:| 滴定次数 | 待测液体积(mL) | 标准盐酸体积(mL) | |
| 滴定前读数(mL) | 滴定后读数(mL) | ||
| 第一次 | 25.00 | 0.00 | 19.90 |
| 第二次 | 25.00 | 0.00 | 20.00 |
| 第三次 | 25.00 | 4.00 | 24.10 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
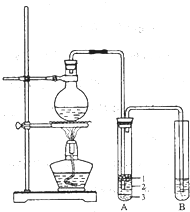 某化学兴趣小组的同学为制取少量溴乙烷,查阅资料得知:
某化学兴趣小组的同学为制取少量溴乙烷,查阅资料得知:| 乙醇 | 溴乙烷 | |
| 状态 | 无色液体 | 无色液体 |
| 密度/g•cm-3 | 0.8 | 1.4 |
| 沸点/℃ | 78.5 | 119.0 |
| 熔点/℃ | -l30 | 38.4 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 煤燃烧是热能转化为化学能的过程 | |
| B. | 动物体内葡萄糖被氧化成CO2是热能转变成化学能的过程 | |
| C. | 植物通过光合作用将CO2转化为葡萄糖是太阳能转变成热能的过程 | |
| D. | 化石燃料属于一次能源,电能属于二次能源 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
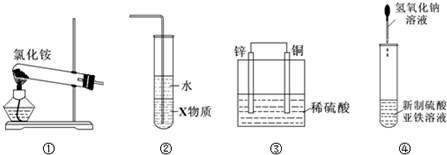
| A. | 实验室用装置①制取氨气 | |
| B. | 装置②中X若为四氯化碳,可用于吸收氨气,并防止倒吸 | |
| C. | 装置③是原电池,锌电极为负极,发生还原反应 | |
| D. | 装置④可用于制备氢氧化亚铁并观察其颜色 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH3CH2Cl与CH3CH2CH2Br | B. | 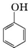 与 与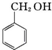 | ||
| C. | 乙酸与HCOOCH3 | D. | CH3CH2CH2OH与CH3OH |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 需加入的试剂 | 操作方法 | |
| CH3CH2OH(水) | 蒸馏 | |
| 乙烷(乙烯) | 洗气 | |
| 乙酸乙酯(乙酸,乙醇) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com