
【题目】在AlCl3和MgCl2的混合溶液中,逐滴加入NaOH溶液直至过量,经测定,加入NaOH的体积和所得沉淀的物质的量的关系如下图所示(b处NaOH的体积为1L),则下列判断错误的是 ( )

A. NaOH的浓度为0.6 mol·L-1 B. 在a点处溶液中的溶质为NaCl
C. 混合溶液中n(Al3+)﹕n(Mg2+)=1﹕1 D. 图中线段oa : ab=4﹕1
【答案】D
【解析】AlCl3和MgCl2的混合溶液中,逐滴加入NaOH溶液,发生反应生成氢氧化铝、氢氧化镁沉淀,加入aLNaOH溶液时,沉淀达最大值共0.2mol,此时溶液为NaCl溶液,继续滴加NaOH溶液直至过量,氢氧化铝与NaOH反应逐渐溶解,在bL时,即再继续滴加NaOH溶液(b-a)L时,氢氧化铝完全溶解,沉淀为氢氧化镁0.1mol,溶液为NaCl、NaAlO2溶液。A、在bL时,溶液为NaCl、NaAlO2溶液,由图象可知:n[Al(OH)3]=0.1mol,n(Mg(OH)2]=0.1mol,根据Mg原子守恒有n(MgCl2)=n(Mg(OH)2]=0.1mol,根据Al原子守恒有n(NaAlO2)=n(AlCl3)=n[Al(OH)3]=0.1mol,由Cl原子守恒有n(Cl)=n(NaCl)=2n(MgCl2)+3n(AlCl3)=2×0.1mol+3×0.1mol=0.5mol,由Na原子守恒有n(NaOH)=n(NaCl)+n(NaAlO2)=0.5mol+0.1mol=0.6mol,所以c(NaOH)= ![]() =0.6mol/L,故A正确;B、加入aLNaOH溶液时,沉淀达最大值共0.2mol,由反应方程式可知,此时溶液为NaCl溶液,故B正确;C、由以上分析可知,溶液中n(MgCl2)=n(Mg(OH)2]=0.1mol,n(AlCl3)=n[Al(OH)3]=0.1mol,即溶液中的混合溶液中n(Al3+):n(Mg2+)=1:1,故C正确;D、加入aLNaOH溶液时,沉淀达最大值共0.2mol,由反应方程式可知,此时溶液为NaCl溶液,在bL时,即再继续滴加NaOH溶液(b-a)L时,氢氧化铝与NaOH恰好反应,氢氧化铝完全溶解,沉淀为氢氧化镁0.1mol,溶液为NaCl、NaAlO2溶液,所以两部分NaOH溶液的体积之比等于消耗的NaOH的物质的量之比,即为n(NaCl)与n(NaAlO2)之比,故oa:ab=a:(b-a)=0.5mol:0.1mol=5:1,故D错误;故选D。
=0.6mol/L,故A正确;B、加入aLNaOH溶液时,沉淀达最大值共0.2mol,由反应方程式可知,此时溶液为NaCl溶液,故B正确;C、由以上分析可知,溶液中n(MgCl2)=n(Mg(OH)2]=0.1mol,n(AlCl3)=n[Al(OH)3]=0.1mol,即溶液中的混合溶液中n(Al3+):n(Mg2+)=1:1,故C正确;D、加入aLNaOH溶液时,沉淀达最大值共0.2mol,由反应方程式可知,此时溶液为NaCl溶液,在bL时,即再继续滴加NaOH溶液(b-a)L时,氢氧化铝与NaOH恰好反应,氢氧化铝完全溶解,沉淀为氢氧化镁0.1mol,溶液为NaCl、NaAlO2溶液,所以两部分NaOH溶液的体积之比等于消耗的NaOH的物质的量之比,即为n(NaCl)与n(NaAlO2)之比,故oa:ab=a:(b-a)=0.5mol:0.1mol=5:1,故D错误;故选D。


 夺冠金卷全能练考系列答案
夺冠金卷全能练考系列答案科目:高中化学 来源: 题型:
【题目】有下列各组物质:
A.O2和O3 B.12C和13C
C.CH3—CH2—CH2—CH3和 ![]()
D.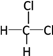 和
和 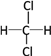 E.甲烷和庚烷
E.甲烷和庚烷
⑴___________组两物质互为同位素;⑵__________组两物质互为同素异形体;
⑶_________组两物质属于同系物;⑷_________组两物质互为同分异构体;
⑸_________组中两物质是同一物质。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定条件下,PbO2与Cr3+反应,产物是Cr2O72-和Pb2+,则与1.0mol Cr3+反应所需PbO2的物质的量为( )
A.3.0mol B.2.5mol C.1.5mol D.0.75mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】分别用浓度均为0.5mol/L的NH3·H2O和NaOH溶液,滴定20mL0.01mol/L Al2(SO4)3溶液,随滴定溶液体积的增大,溶液的导电能力变化曲线如图所示,下列说法中正确的是
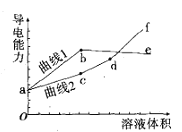
A. 曲线2 代表滴加NH3·H2O溶液的变化曲线
B. b和d点对应的溶液均显碱性
C. b点溶液中c(NH4+)>c(SO42-)>c(H+)>c(OH-)
D. df段导电能力升高的原因是发生了反应Al(OH)3+OH-=[Al(OH)4]-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是 ( )
A. ![]() 比
比![]() 沸点高
沸点高
B. O2-半径比![]() 的小
的小
C. Na和Cs属于第IA族元素,Cs失电子能力比Na的强
D. P和As属于第VA族元素, ![]() 酸性比
酸性比![]() 的弱
的弱
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某溶液含有HCO3-、CO32-、SO32-、NO3-中的5种离子,若向其中加入Na2O2粉末,充分反应后(溶液体积变化忽略不计),溶液中离子浓度保持不变是( )
A.NO3- B.CO32-、 NO3- C.SO32-、NO3- D.CO32-、Na+、NO3-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图所示为某化学兴趣小组设计的乙醇催化氧化及其产物检验的实验装置(图中加热仪器、铁架台、铁夹等均未画出)。

图中:A为无水乙醇(沸点为78℃),B为绕成螺旋状的细铜丝或银丝,C为无水CuSO4粉末,D为碱石灰,F为新制的碱性Cu(OH)2悬浊液。
(1)在上述装置中,实验时需要加热的仪器为(填仪器或某部位的代号) _____________________。
(2)为使A中乙醇平稳气化成乙醇蒸气,常采用的方法是_____________。
(3)检验乙醇氧化产物时F中的实验现象是____________________________。
(4)E处是一种纯净物,其反应方程式为_______________________________________。
(5)写出乙醇发生催化氧化的化学方程式_______________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NA为阿伏加德罗常数,下列说法正确的是( )
A. 标准状况下,11.2L的戊烷所含的分子数大于0.5NA
B. 28g乙烯所含共用电子对数目为4NA
C. 标准状况下,11.2L二氯甲烷所含分子数为0.5NA
D. 现有乙烯、丙烯、丁烯的混合气体共14g,其原子数为2NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】天然维生素P(结构如图)存在于槐树花蕾中,它是一种营养增补剂。关于维生素P的叙述正确的是:

A. 若R为甲基则该物质的分子式可以表示为C16H10O7 B. 分子中有三个苯环
C. lmol该化合物与NaOH溶液作用消耗NaOH的物质的量以及与氢气加成所需的氢气的物质的量分别是4 mol、8 mol D. lmol该化合物最多可与7molBr2完全反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com