
【题目】水中加入下列物质,对水的电离平衡不产生影响的是
A. NaHCO3 B. NaBr C. KAl(SO4)2 D. NH3
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】如右图,将铁棒和石墨棒插入盛有饱和NaCl溶液的U型管中,下列分析正确的是
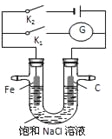
A. K1闭合,铁棒上发生的反应为2H++2e-=H2↑
B. K1闭合,石墨棒周围溶液pH逐渐升高
C. K2闭合,铁棒不会被腐蚀,属于牺牲阳极的阴极保护法
D. K2闭合,电路中通过0.002 NA个电子时,两极共产生0.001 mol气体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列属于放热反应的是( )
A. 铝热反应 B. 煅烧石灰石(CaCO3)制生石灰(CaO)
C. C与CO2共热 D. Ba(OH)2·8H2O晶体与NH4Cl晶体反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质的转化必须加入氧化剂且通过一步反应就能完成的是 ( )
①NO2→NO ②NO2→HNO3 ③N2→NO2 ④N2→NO ⑤N2→NH3
A. ① B. ②⑤ C. ④ D. ③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列烯烃和H2O发生加成反应所得产物有同分异构体的是( )
A. CH3CH=CH2 B. CH3CH=CHCH3
C. CH2=CH2 D. (CH3)2C=C(CH3)2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碳元素及其化合物与人类的生活、生产息息相关,请回答下列问题:
(1)绿色植物的光合作用吸收CO2释放O2的过程可以描述为以下两步:
2CO2(g)+2H2O(l)+2C5H10O4(s) = 4(C3H6O3)+(s)+O2(g)+4e- △H=+1360 kJ·mol-1
12(C3H6O3)+(s)+12e-= C6H12O6(s,葡萄糖)+6C5H10O4(s)+3O2(g) △H=-1200 kJ·mol-1
则绿色植物利用二氧化碳和水合成葡萄糖并放出氧气的热化学方程式为:_________。
(2)工业炼铁时有如下副反应:Fe(s)+CO2(g)![]() FeO(s)+CO(g) △H>0,该反应能正向自发进行的原因是_________________。某温度时,把Fe和CO2放入体积固定的容器中,CO2 的起始浓度为2.0 molL-1,达到平衡后,CO的浓度为1.0 molL-1,则该温度下,该反应的平衡常数K=___________。如果平衡后,再通入一定量的CO,则CO2的物质的量分数将________________。(填编号)
FeO(s)+CO(g) △H>0,该反应能正向自发进行的原因是_________________。某温度时,把Fe和CO2放入体积固定的容器中,CO2 的起始浓度为2.0 molL-1,达到平衡后,CO的浓度为1.0 molL-1,则该温度下,该反应的平衡常数K=___________。如果平衡后,再通入一定量的CO,则CO2的物质的量分数将________________。(填编号)
A.增大 B.减少 C.不变
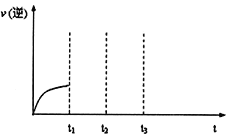
(3)己知反应Fe(s)+CO2(g)![]() FeO(s)+CO(g) △H>0的逆反应速率随时间变化的关系如下图,ti—升温,t2—达到平衡,请在图上画出ti—t3时的v(逆)的变化曲线。_______
FeO(s)+CO(g) △H>0的逆反应速率随时间变化的关系如下图,ti—升温,t2—达到平衡,请在图上画出ti—t3时的v(逆)的变化曲线。_______
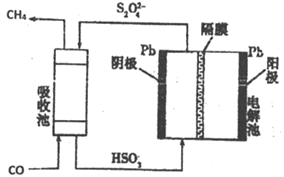
(4)用间接化学法除去CO的过程如下图所示:己知电解池的阴极室中溶液的pH在4—6之间,写出阴极的电极反应式 ____________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在下图点滴板上进行四个溶液间反应的小实验,其对应反应的离子方程式书写正确的是( )

A. a反应:Fe2++2H++H2O2===Fe3++2H2O
B. b反应:HCO![]() +OH-===CO
+OH-===CO![]() +H2O
+H2O
C. c反应:H++OH-===H2O
D. d反应:Al3++3NH3·H2O===Al(OH)3↓+3NH![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据图判断,下列说法正确的是
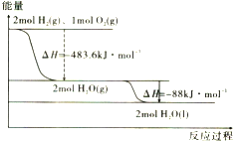
A. 2H2(g)+O2(g)=2H2O(g) △H1>0
B. 氢气的燃烧热为△H2= -241. 8kJ/mol
C. 上述A、B选项中的△H1>△H2
D. 液态水分解的热化学方程式为2H2O(l)= 2H2(g)+O2(g) △H=+571.6kJ/mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定条件下,发生反应:2X(g)+Y(g) ![]() 2Z(g) ΔH=-197kJ·mol-1,若将2mol X和1mol Y充入2L的恒容密闭容器中,反应10min,测得X的物质的量为1.4mol,下列说法正确的是( )
2Z(g) ΔH=-197kJ·mol-1,若将2mol X和1mol Y充入2L的恒容密闭容器中,反应10min,测得X的物质的量为1.4mol,下列说法正确的是( )
A.10min内,反应放出的热量为197kJ热量
B.10min内,X的平均反应速率为0.06mol·L-1·min-1
C.第10min时,Y的反应速率小于0.015mol·L-1·min-1(假如体系温度不变)
D.第10min时,Z浓度为0.6mol·L-1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com