
| A. | Na2CO3比NaHCO3热稳定性强 | |
| B. | 相同质量的Na2CO3和NaHCO3与足量盐酸作用时,产生的气体质量相同 | |
| C. | 相同温度下,Na2CO3的溶解度小于NaHCO3 | |
| D. | 物质的量浓度相同时,Na2CO3溶液的pH比NaHCO3溶液的小 |
分析 A.碳酸氢钠受热易分解;
B.利用n=$\frac{m}{M}$,可计算物质的量,因酸足量,利用Na2CO3~CO2,NaHCO3~CO2来分析;
C.相同条件下,碳酸氢钠的溶解度小;
D.Na2CO3水解程度比NaHCO3大.
解答 解:A.碳酸氢钠受热易分解,不稳定,则Na2CO3比NaHCO3热稳定性强,故A正确;
B.设质量都是106g,则Na2CO3和NaHCO3的物质的量分别为1mol、$\frac{106}{84}$mol,根据Na2CO3~CO2,NaHCO3~CO2,产生的CO2的物质的量分别为1mol、$\frac{106}{84}$mol,所以产生的气体质量不同,故B错误;
C.Na2CO3和NaHCO3在相同条件下,碳酸氢钠的溶解度小,则在水中的溶解度为:Na2CO3>NaHCO3,故C错误;
D.Na2CO3水解程度比NaHCO3大,物质的量浓度相同时,碳酸钠溶液碱性较大,则物质的量浓度相同时,Na2CO3溶液的pH比NaHCO3溶液的大,故D错误;
故选:A.
点评 本题考查碳酸钠和碳酸氢钠的性质,涉及溶解度、稳定性、与酸的反应等,注意与酸反应中量少的物质完全反应,题目难度不大.


 小学教材完全解读系列答案
小学教材完全解读系列答案科目:高中化学 来源: 题型:实验题
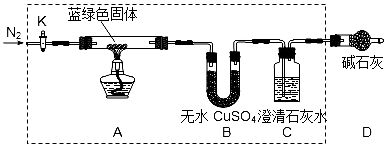
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ${\;}_{118}^{175}$X | B. | ${\;}_{175}^{118}$X | C. | ${\;}_{118}^{293}$X | D. | ${\;}_{293}^{118}$X |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
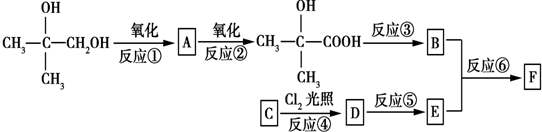
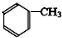 ,反应③的条件是浓硫酸、加热.
,反应③的条件是浓硫酸、加热.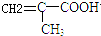 $\stackrel{一定条件}{→}$
$\stackrel{一定条件}{→}$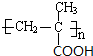 .
.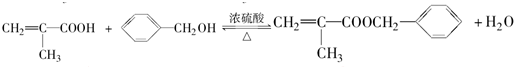 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 某反应由两步反应 A、B、C 构成,它的反应能量曲线如图所示(E1、E2、E3、E4表示活化能).回答下列问题
某反应由两步反应 A、B、C 构成,它的反应能量曲线如图所示(E1、E2、E3、E4表示活化能).回答下列问题查看答案和解析>>
科目:高中化学 来源: 题型:选择题
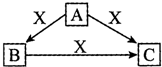 A、B、C、X均为中学化学常见的物质,一定条件下,它们有如下转化关系(部分产物已略去),下列说法错误的是( )
A、B、C、X均为中学化学常见的物质,一定条件下,它们有如下转化关系(部分产物已略去),下列说法错误的是( )| A. | 若X为Cl2,则C可能为FeCl3 | |
| B. | 若X为KOH溶液,则A可能为AlCl3溶液 | |
| C. | 若X为Fe,则A可能为HNO3 | |
| D. | 若A、B、C均为焰色反应呈黄色的化合物,则X可能为CO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com