
【题目】(化学——选修5:有机化学基础)(15分)
有机化合物G是合成维生素类药物的中间体,其结构简式如图所示

G的合成路线如下图所示:

其中A~F分别代表一种有机化合物,合成路线中部分产物及反应条件已略去
已知:
请回答下列问题:
(1)G的分子式是 ,G中官能团的名称是 ;
(2)第②步反应的化学方程式是 ;
(3)B的名称(系统命名)是 ;
(4)第②~⑥步反应中属于取代反应的有 (填步骤编号);
(5)第④步反应的化学方程式是 ;
(6)写出同时满足下列条件的E的所有同分异构体的结构简式 。
①只含一种官能团;②链状结构且无-O-O-;③核磁共振氢谱只有2种峰。
【答案】(1)C6H10O3;酯基和羟基 (2)(CH3)2CH CH2Br+NaOH![]() (CH3)2CH CH2OH+NaBr
(CH3)2CH CH2OH+NaBr
(3):2-甲基-1-丙醇 (4)②⑤ (5)
(6)CH3COOCH2CH2OOCCH3、CH3CH2OOCCOOCH2CH3、CH3OOCCH2CH2COOCH3
【解析】
根据反应③的产物可知A为![]() ,反应③为醇的氧化,根据G推知F为
,反应③为醇的氧化,根据G推知F为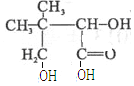 ,结合已知和反应⑤有乙醇产生推得C为
,结合已知和反应⑤有乙醇产生推得C为![]() ,反应④类似所给已知反应,则E为
,反应④类似所给已知反应,则E为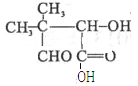 ,根据E的结构可知它含三种官能团,而它的同分异构体含一种官能团,可能是羧基或酯基,只有2中氢,应该有对称结构,有如下几种:CH3COOCH2CH2OOCCH3、CH3OOCCH2CH2COOCH3、CH3CH2OOCCOOCH2CH3
,根据E的结构可知它含三种官能团,而它的同分异构体含一种官能团,可能是羧基或酯基,只有2中氢,应该有对称结构,有如下几种:CH3COOCH2CH2OOCCH3、CH3OOCCH2CH2COOCH3、CH3CH2OOCCOOCH2CH3


 云南师大附小一线名师提优作业系列答案
云南师大附小一线名师提优作业系列答案 冲刺100分单元优化练考卷系列答案
冲刺100分单元优化练考卷系列答案科目:高中化学 来源: 题型:
【题目】用NA表示阿伏伽德罗常数值,下列叙述中正确的是
A. 5.6g铁在足量的O2中燃烧,转移的电子数为0.3NA
B. 18g H218O和D2O的混合物中,所含中子数为9NA
C. 1molFe分别与足量的稀硫酸和稀硝酸反应转移电子数均为2 NA
D. 0.4 mol NH3与0.6 mol O2在催化剂的作用下充分反应,得到NO的分子数为0.4NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某课外活动小组利用如图1装置进行乙醇的催化氧化实验并制取乙醛(试管丁中用水吸收产物),图中铁架台等装置已略去,实验时,先加热玻璃管中的镀银铜丝,约lmin后鼓入空气,请填写下列空白:

(1)检验乙醛的试剂是__;
A、银氨溶液 B、碳酸氢钠溶液 C、新制氢氧化铜 D、氧化铜
(2)乙醇发生催化氧化的化学反应方程式为____________;
(3)实验时,常常将甲装置浸在70℃~80℃的水浴中,目的是_____________,由于装置设计上的陷,实验进行时可能会____________;
(4)反应发生后,移去酒精灯,利用反应自身放出的热量可维持反应继续进行,进一步研究表明,鼓气速度与反应体系的温度关系曲线如图2所示,试解释鼓气速度过快,反应体系温度反而下降的原因________,该实验中“鼓气速度”这一变量你认为__________________可用来估量;
(5)该课外活动小组偶然发现向溴水中加入乙醛溶液,溴水褪色,该同学为解释上述现象,提出两种猜想:①溴水将乙醛氧化为乙酸;②溴水与乙醛发生加成反应,请你设计一个简单的实验,探究哪一种猜想正确______________________________?
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】最早使用的化学电源是锌锰电池,即大家所熟悉的干电池(dry cell),其结构如下图所示:尽管这种电池的历史悠久,但对它的电化学过程尚未完全了解。一般认为,放电时,电池中的反应如下:

E极:2MnO2+2H2O+2e-="==" 2MnO(OH)+2OH-
F极:Zn+2NH4Cl -2e-=== Zn(NH3)2Cl2+2H+
总反应式:2MnO2+Zn+2NH4Cl ="==" 2MnO(OH)+Zn(NH3)2Cl2
下列说法正确的是
A. E极是电池的正极,发生的是氧化反应
B. F极是电池的负极,发生的是氧化反应
C. 从结构上分析,锌锰电池应属于可充电电池
D. 锌锰电池内部发生的氧化还原反应是可逆的
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将纯锌片和纯铜片按图方式插入100 mL相同浓度的稀硫酸中一段时间,请回答下列问题:

(1)下列说法正确的是________。
A.甲、乙均为化学能转变为电能的装置
B.乙中铜片上没有明显变化
C.甲中铜片质量减少、乙中锌片质量减少
D.两烧杯中溶液的pH均增大
(2)在相同时间内,两烧杯中产生气泡的速度:甲____乙(填“>”、“<“或“=”)。
(3)当甲中产生1.12L(标准状况)气体时,通过导线的电子数目为__________。
(4)当乙中产生1.12L(标准状况)气体时,将锌、铜片取出,再将烧杯中的溶液稀释至1 L,测得溶液中c(H+)=0.1 mol·L-1(设反应前后溶液体积不变)。试确定原稀硫酸的物质的量浓度为______。
(5)利用下列反应:Fe+2Fe3+=3Fe2+制一个化学电池(给出若干导线和一个小灯泡,电极材料和电解液自选),画出实验装置图,注明电解质溶液名称和正负极材料,标出电流方向,写出电极反应式。___

_______是正极,正极反应式:_____________;
________是负极,负极反应式:____________
(6)1958年世界上第一个心脏起搏器在瑞典植入人体成功,使用寿命长达10年之久。这种能源起搏器中安装寿命最长、可靠性最高的锂一碳电池,这种电池容量大,电压稳定,能在-56.7~71.1℃温度范围内正常工作。现已在火箭、移动电话、笔记本电脑中广泛使用。它采用锂和石墨作电极,四氯化铝锂(LiAlCl4)溶解在亚硫酰氯中(SOCl2)组成电解质溶液。电池总反应为:8Li+3SOCl2=6LiCl+Li2SO3+2S,此电池中__作正极,负极的电极反应为_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为了探究实验室制氯气过程中反应物与生成氯气之间量的关系,设计了如下图所示的装置。

(1)装置A的名称是_____________________。
(2)该实验装置检查气密性的方法是________________________________。
(3)如果将过量二氧化锰与20mL 12mol/L的盐酸混合加热,充分反应后收集到的氯气少于0.06mol,其可能原因有__________
a.加热使浓盐酸挥发出大量HCl b.盐酸变稀后不发生该反应
c.烧瓶中残留有氯气 d.装置B中液面高于A
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物G是一种“β-兴奋剂”,其合成路线如下:

已知:


(1)写出化合物E同时符合下列条件的所有同分异构体的结构简式___________
①红外光谱显示含有三种官能团,其中无氧官能团与E相同,不含甲基
②1H—NMR谱显示分子中含有苯环,且苯环上只有一种不同化学环境的氢原子。
③苯环上只有4个取代基,能发生银镜反应
(2)下列说法不正确的是__________
A.化合物B生成C的反应为取代反应
B.1mol化合物D最多与4molH2发生加成反应
C.化合物D生成E的条件为浓氯水/铁屑
D.化合物G的分子式为C17H14Cl2NO3
(3)写出E+F→G的化学方程式________________________________________________
(4)根据题中信息,设计以苯和CH3COCl为原料制备F的合成路线(用流程图表示,其他无机试剂任选)__________________________________________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示,两电极一为碳棒,一为铁片,若电流表的指针发生偏转,且a极上有大量气泡生成,则以下叙述正确的是

A. a为负极,是铁片,烧杯中的溶液为硫酸
B. b为负极,是铁片,烧杯中的溶液为硫酸铜溶液
C. a为正极,是碳棒,烧杯中的溶液为硫酸
D. b为正极,是碳棒,烧杯中的溶液为硫酸铜
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向含 S2-、 Fe2+、 Br -、 I-各 0.1 mol 的溶液中通入 Cl2, 通入 Cl2 的体积(标准状况) 和溶液中相关离子的物质的量的关系图正确的是

A. A B. B C. C D. D
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com