
【题目】NA表示阿伏加德罗常数的值。下列说法正确的是
A. 电解精炼Cu时,导线中通过2NAe-时,阳极质量一定减少64 g
B. 标准状况下,0.1 mol Cl2溶于水,转移的电子数目为0.1NA
C. 标准状况下,11.2 LCHCl3中含有的共用电子对数目为2NA
D. 12.0 g熔融的NaHSO4中含有离子总数为0.2NA
科目:高中化学 来源: 题型:
【题目】有4种碳架如下的烃,下列说法正确的是 ( )
① ![]() 和
和![]() 是同分异构体 ②
是同分异构体 ② ![]() 和
和![]() 是同系物
是同系物
③ ![]() 和
和![]() 都能发生加成反应 ④
都能发生加成反应 ④![]() 、
、![]() 、
、![]() 、
、![]() 都能发生取代反应
都能发生取代反应
A. ①④B. ①②C. ①②③D. ①②④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,下列有关叙述中不正确的是
A. pH=13的NaOH溶液与pH=1的醋酸溶液等体积混合后所得溶液的pH<7
B. 沉淀溶解平衡:BaSO4(s)![]() Ba2+(aq)+SO42-(aq)的Ksp为1.1×10-10,说明BaSO4是弱电解质
Ba2+(aq)+SO42-(aq)的Ksp为1.1×10-10,说明BaSO4是弱电解质
C. 在0.10molL﹣1的NH3H2O溶液中加入少量NH4Cl晶体,则NH3H2O电离被抑制,溶液pH减少
D. 0.1mol L-1的HA溶液pH=1,该溶液中由水电离的c(OH-)=l×10-13mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列体系中,离子可能大量共存的是( )
A.滴加KSCN显红色的溶液:NH、K+、Cl-、HCO
B.常温,水电离出的c(H+)=1×10-12 mol/L的溶液:Fe2+、Mg2+、SO![]() 、NO
、NO
C.使酚酞试剂显红色的溶液:Na+、Ba2+、NO、[Al(OH)4]-
D.加入Al能产生H2的溶液:K+、NH、CH3COO-、Cl-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某新型纳米材料的主要成分为MFe2Ox(3<x<4),其中M表示+2价的金属元素,下列说法正确的是( )
A.MFe2Ox中铁元素的化合价一定为+2B.320g MFe2Ox的物质的量大于2mol
C.1mol MFe2Ox中Fe的质量为112 gD.1mol MFe2Ox的体积为22.4 L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将8.4g Fe投入浓硝酸中,产生红棕色气体A,把所得溶液减压蒸干,得到30g Fe(NO3)2和Fe(NO3)3的混合物,将该固体隔绝空气在高温下加热,得到红棕色的Fe2O3和气体B,A、B气体混合通入足量水中得到硝酸和NO,在标准状况生成NO气体的体积为
A. 1120mL B. 2240mL C. 3360mL D. 4480mL
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上用电解法可用于治理亚硝酸盐对水体的污染,模拟工艺如图所示,下列说法不正确的是
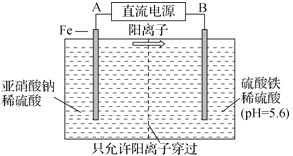
A. A、B分别为直流电源的正极和负极
B. 当电解过程转移0.6mol电子时,左侧区域质量减少1.4g
C. 电解过程中,左侧区域将依次发生反应为:Fe-2e-=Fe2+ 、2NO2-+8H++6Fe2+=N2↑+6Fe3++4H2O
D. 研究表明,当右侧区域pH较小时,会有气体逸出,该现象说明H+的氧化性强弱与其c(H+)有关
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在同温同压下,在两个容积相同的容器中,一个盛有CO2气体,另一个盛有O2和N2的混和气体,则两容器内的气体一定具有相同的( )
A.密度B.原子数C.质量D.分子数
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某研究小组对碘化钾溶液在空气中发生氧化反应的速率进行实验探究。
(初步探究)
示意图 | 序号 | 温度 | 试剂A | 现象 |
| ① | 0℃ | 0.5 mol·L-1稀硫酸 | 4min左右出现蓝色 |
② | 20℃ | 1min左右出现蓝色 | ||
③ | 20℃ | 0.1 mol·L-1 稀硫酸 | 15min左右出现蓝色 | |
④ | 20℃ | 蒸馏水 | 30min左右出现蓝色 |
(1)为探究温度对反应速率的影响,实验②中试剂A应为_______ 。
(2)写出实验③中I-反应的离子方程式___________。
(3)对比实验②③④,可以得出的结论是__________。
(继续探究)溶液pH对反应速率的影响
查阅资料:
i.pH<11.7时,I-能被O2氧化为I2。
ii.pH>9.28时,I2发生歧化反应:3I2+6OH-=IO3-+5I-+3H2O,pH越大,歧化速率越快
(4)小组同学用4支试管在装有O2储气瓶中进行实验,装置如图所示:
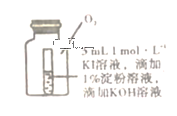
序号 | ⑤ | ⑥ | ⑦ | ⑧ |
试管中溶液的pH | 8 | 9 | 10 | 11 |
放置10小时后的现象 | 出现蓝色 | 颜色无明显变化 | ||
pH为10、11时,试管⑦和⑧中颜色无明显变化的原因是________(填序号)。
A.既发生氧化反应又发生歧化反应,歧化反应速率大于氧化反应速率和淀粉变色速率
B.既发生氧化反应又发生歧化反应,歧化反应速率小于氧化反应速率和淀粉变色速率
C.发生了氧化反应,但没有发生歧化反应
D.发生了歧化反应,但没有发生氧化反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com