
(共14分)氮是地球上含量丰富的一种元素,氮及其化合物在工农业生产、生活中有着重要作用,合成氨工业在国民生产中有重要意义。以下是关于合成氨的有关问题,请回答:
(1)若在一容积为2L的密闭容器中加入0.2 molN2;的和0.6 molH2的,在一定条件下发生反应: ,若在5分钟时反应达到平衡,此时测得NH3 的物质的量为0.2 mol。则前5分钟的平均反应速率v( N2)=____。
,若在5分钟时反应达到平衡,此时测得NH3 的物质的量为0.2 mol。则前5分钟的平均反应速率v( N2)=____。
(2)平衡后,若要提高H2的转化率,可以采取的措施有______。
A.加了催化剂 B.增大容器体积
C.降低反应体系的温度 D.加入一定量氮气
(3)若在0.5 L的密闭容器中,一定量的氮气和氢气进行如下反应:
 ,其化学平衡常数K与温度T的关系如表所示:
,其化学平衡常数K与温度T的关系如表所示:
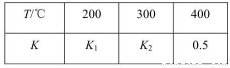
请完成下列问题:
①试比较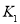 、
、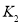 的大小,
的大小,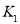 ____
____ 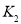 (填“<”、“>”或“=”):
(填“<”、“>”或“=”):
②下列各项能作为判断该反应达到化学平衡状态的依据是____(填序号字母)
A.容器内 N2、H2、NH3的物质的量浓度之比为1:3:2
B.
C.容器内压强保持不变
D.混合气体的密度保持不变
③400℃时,反应 的化学平衡常数为____。当测得NH3、N2和H2 物质的量分别为3 mol、2 mol和1 mol时,则该反应的
的化学平衡常数为____。当测得NH3、N2和H2 物质的量分别为3 mol、2 mol和1 mol时,则该反应的 (填“<”、“>”或“=”)。
(填“<”、“>”或“=”)。
(4)根据化学反应速率和化学平衡理论,联系合成氨的生产实际,你认为下列说法不正确的是____。
A.化学反应速率理论可指导怎样在一定时间内快出产品
B.勒夏特列原理可指导怎样使用有限原料多出产品
C.催化剂的使用是提高产品产率的有效方法
D.正确利用化学反应速率和化学反应限度理论都可以提高化工生产的综合经济效益
(1)0.01mol·L-1·min-1 (2)C、D
(3)①>② BC ③ 2 > (4) C
【解析】
试题分析:(1)根据化学反应方程式,在5分钟时,生成NH3 的物质的量为0.2 mol,则氮气反应掉0.1mol,则前5分钟的平均反应速率v( N2)=0.1mol/(5min·2L)= 0.01mol·L-1·min-1 ;
(2) A.加入催化剂,不影响平衡,氢气转化率不变,错误;B.增大容器体积,平衡逆向移动,氢气的转化率降低,错误;C.降低反应体系的温度,平衡正向移动,氢气的转化率增大,正确;D.加入一定量氮气,加入氮气,平衡正向移动,氢气的转化率增大,正确;选CD。
(3)①因工业合成氨是放热反应,升高温度平衡向左移动,反应程度减小,K1>K2;
②A.容器中N2、H2、NH3的浓度之比与反应是否达到平衡状态无关,错误;B.可逆反应达到平衡状态时,v(正)=v(逆),且化学反应速率之比等于化学计量数之比,反应平衡时,3v正(N2)=v逆(H2),说明反 应达到平衡状态,正确;C.因反应前后气体总体积发生变化,压强不变,说明反应混合物中各组分的含量不变,即反应处于平衡状态,正确;D.反应前后气体质量不变,容器容积不变,反应过程中混合气体的密度一直保持不变;不能说明反应达到平衡状态,错误;选BC;
③根据可逆反应,平衡常数互为倒数,在400℃时,合成氨反应N2(g)+3H2(g) 2NH3(g)的化学平衡常数K=0.5,则2NH3(g)
2NH3(g)的化学平衡常数K=0.5,则2NH3(g) N2(g)+3H2(g)的化学平衡常数为2;利用容器中各物质的物质的量浓度可知Q=62/(4×23)=1.125>2,平衡正向移动,v(正)>v(逆)。
N2(g)+3H2(g)的化学平衡常数为2;利用容器中各物质的物质的量浓度可知Q=62/(4×23)=1.125>2,平衡正向移动,v(正)>v(逆)。
(4)催化剂不能提高转化率,只能改变化学反应速率,缩短反应时间,选C。
考点:考查化学反应速率的计算,影响平衡的因素,化学平衡状态的判断,化学平衡常数等知识。


科目:高中化学 来源:2013-2014广东省东莞市高一上学期期末化学A试卷(解析版) 题型:选择题
下列离子方程式中,正确的
A.向AlCl3溶液中逐渐滴入NaOH溶液至过量:Al3++4OH-=AlO2-+2H2O
B.将碳酸钙加入过量盐酸中:CO32-+2H+=CO2↑+H2O
C.向氯化铁溶液中加入铁粉:2Fe3++Fe=3Fe2+
D.在CuSO4溶液中加入Ba(OH)2溶液:Ba2+ + SO42-= BaSO4↓
查看答案和解析>>
科目:高中化学 来源:2014-2015四川省广安市高一期末考试化学试卷(解析版) 题型:选择题
下列各组中的两物质相互反应时,与反应条件和用量无关的是
A.Na和O2 B.Fe和FeCl3
C.CO2和NaOH D.AlCl3和NaOH
查看答案和解析>>
科目:高中化学 来源:2014-2015四川省广安市高一期末考试化学试卷(解析版) 题型:选择题
青铜是我国使用最早的合金。下列关于青铜性质的说法,不正确的是
A.熔点比纯铜低 B.能够导电 C.能够导热 D.硬度比纯铜小
查看答案和解析>>
科目:高中化学 来源:2014-2015山东省聊城市茌平等三县高二上学期期末联考化学试卷(解析版) 题型:选择题
已建立平衡的某可逆反应,当改变条件使化学平衡向正反应方向移动时,下列叙述正确的是
①生成物的体积分数一定增加②生成物的产量一定增加
③反应物的转化率一定增加④反应物的浓度一定降低⑤正反应速率一定大于逆反应速率
A.①②④⑤ B.①②③⑤
C.②③ D.②⑤
查看答案和解析>>
科目:高中化学 来源:2014-2015山东省聊城市茌平等三县高二上学期期末联考化学试卷(解析版) 题型:选择题
下列说法正确的是
A.任何化学反应都可以设计成电解池反应
B.电镀铜和电解精炼铜时,电解质溶液中的c( Cu2+)均保持不变
C.电解冶炼镁、铝通常电解MgCl2 和Al2O3 ,也可电解MgO和AlCl3
D.若把Cu+H2SO4 =CuSO4 +H2↑设计成电解池,应用Cu作阳极
查看答案和解析>>
科目:高中化学 来源:2014-2015山东省菏泽市高一上学期期末考试化学A试卷(解析版) 题型:实验题
(12分)实验室需要配制0.1 mol/L NaOH溶液450 mL,回答下列问题:
(1)如图所示的仪器中配制溶液肯定不需要的是 (填序号),配制上述溶液还需用到的玻璃仪器是 (填仪器名称)
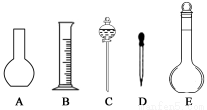
(2)下列操作中,容量瓶所具备的功能有 (填序号)。
A.贮存溶液
B.配制一定体积准确浓度的标准溶液
C.测量容量瓶规格以下的任意体积的液体
D.用来加热溶解固体溶质
(3)根据计算用托盘天平称取NaOH的质量为 g;
(4)取用任意体积的所配0.1 mol/L NaOH溶液时,下列物理量中不随所取体积的多少而变化的是(填字母) ;
A.溶液中NaOH的物质的量 B.溶液的浓度
C.溶液中Na+的数目 D.溶液的密度
(5)将所配制的NaOH溶液进行测定,发现浓度大于0.1 mol/L。请你分析下列哪些操作会引起所配浓度偏大(填写字母) 。
A.烧杯未进行洗涤
B.配制前,容量瓶中有少量蒸馏水
C.NaOH在烧杯中溶解后,未冷却就立即转移到容量瓶中,并进行定容;
D.往容量瓶转移时,有少量液体溅出
E.在容量瓶中定容时俯视容量瓶刻度线
F.定容后塞上瓶塞反复摇匀,静置后,液面不到刻度线,再加水至刻度线。
查看答案和解析>>
科目:高中化学 来源:2014-2015江西省高一上学期期末化学试卷(解析版) 题型:填空题
(8分)已知A、B、C、D分别是AlCl3、BaCl2、FeSO4、NaOH四种化合物中的一种,它们的水溶液之间的一些反应现象如下:
①A + B→白色沉淀,加入稀硝酸,沉淀不溶解
②B + D→白色沉淀,在空气中放置,沉淀由白色转化为红褐色
③C + D→白色沉淀,继续加入D溶液,白色沉淀逐渐消失
(1)试推断A B C D (化学式)。
(2)写出下列反应的化学方程式或离子方程式:
①实验②中沉淀由白色转化为红褐色的化学方程式 ,
②C溶液与D溶液反应后生成的白色沉淀溶解于D溶液中的离子方程式 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com