
| A、盐酸 | B、醋酸 | C、蒸馏水 | D、氨水 |


 单元期中期末卷系列答案
单元期中期末卷系列答案科目:高中化学 来源: 题型:
| A、在常温常压下,11.2LN2含有的分子数小于0.5NA |
| B、标准状况下,2.24LSO3含有的原子数为0.4NA |
| C、将1L 2 mol/L的FeCl3溶液制成胶体后,其中含有氢氧化铁胶粒数为2NA |
| D、46gNO2和N2O4混合气体所含氧原子数目有可能为3NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
 如图是琥珀酸亚铁片的部分说明书,已知Fe2+在空气中很容易被氧化为Fe3+,下列关于该药物的说法不正确的是( )
如图是琥珀酸亚铁片的部分说明书,已知Fe2+在空气中很容易被氧化为Fe3+,下列关于该药物的说法不正确的是( )| A、与维生素C同服,可增加本品的吸收,是因为维生素C具有还原性 |
| B、除去该药片的包衣膜后,将药物溶于水溶液为无色 |
| C、可用碘水检验该药片中是否含有淀粉 |
| D、薄膜包衣预混剂作用是防止亚铁盐被空气中的氧气氧化 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、碳酸氢钙溶液中滴加少量的氢氧化钠溶液:Ca2++HCO3-+OH-=CaCO3↓+H2O | ||||
| B、金属铝与稀硝酸反应:2Al+6H+=2Al3++3H2↑ | ||||
C、向NH4HCO3溶液中加过量NaOH溶液并加热:NH4++OH-
| ||||
| D、碳酸氢铵溶液中加入过量稀盐酸:CO32-+2H+=CO2↑+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、甲烷和氯气取代:CH4+Cl2
| |||
B、乙烯和水加成:CH2=CH2+H2O
| |||
C、苯酚钠溶液中通少量CO2:CO2+H2O+ → →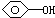 +HCO3- +HCO3- | |||
D、实验室用液溴和苯在催化剂作用下制溴苯: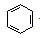 +Br2 +Br2
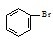 +HBr +HBr |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、苯酚钠溶液中通入少量CO2 2C6H5ONa+CO2+H2O→2C6H5OH+Na2CO3 | ||
B、乙酸乙酯在酸性条件下水解 CH3COOCH2CH3+H218O
| ||
C、溴乙烷的消去反应 C2H5Br+NaOH
| ||
D、乙醛和银氨溶液反应 CH3CHO+2Ag(NH3)2OH
|
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
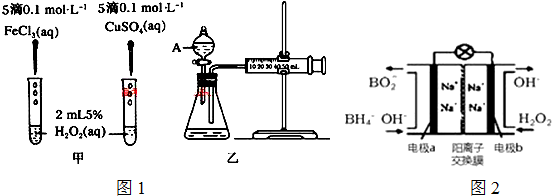
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com