
下列离子的检验方法合理的是( )
A.向某溶液中滴入KSCN溶液呈血红色,说明不含Fe2+
B.向某溶液中通入Cl2,然后再加入KSCN溶液变血红色,说明原溶液中含有Fe2+
C.向某溶液中加入NaOH溶液,得到红褐色沉淀,说明溶液中含有Fe3+
D.向某溶液中加入NaOH溶液得白色沉淀,又观察到颜色逐渐变为红褐色,说明溶液中只含有Fe2+,不含有Mg2+
科目:高中化学 来源: 题型:
在重水D2O中存在电离:D2O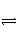
 D++OD-,因此,对D2O可以采用同pH一样的定义来规定pD,即pD=-lg[D+]。已知在某温度下,D2O达电离平衡时,[D+][OD-]=1.6×10-15 mol2·L-2,则纯净的D2O在此温度下的pD________7(填“>”、“<”或“=”)。此温度下,若用0.01 mol DCl溶于D2O配成1 L溶液,pD________;若用0.01 mol NaOD溶于D2O配成1 L溶液时,pD________12(填“>”、“<”或“=”)。
D++OD-,因此,对D2O可以采用同pH一样的定义来规定pD,即pD=-lg[D+]。已知在某温度下,D2O达电离平衡时,[D+][OD-]=1.6×10-15 mol2·L-2,则纯净的D2O在此温度下的pD________7(填“>”、“<”或“=”)。此温度下,若用0.01 mol DCl溶于D2O配成1 L溶液,pD________;若用0.01 mol NaOD溶于D2O配成1 L溶液时,pD________12(填“>”、“<”或“=”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列反应,其产物的颜色按红色、红褐色、淡黄色、蓝色顺序排列的是( )
①金属钠在纯氧中燃烧 ②FeSO4溶液中滴入NaOH溶液,并在空气中放置一段时间
③FeCl3溶液中滴入KSCN溶液 ④无水硫酸铜放入医用酒精中
A.②③①④ B.③②①④
C.③①②④ D.①②③④
查看答案和解析>>
科目:高中化学 来源: 题型:
甲、乙、丙三种物质之间有如下转化关系:
甲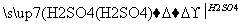 乙
乙 丙
丙 甲
甲
(1)若甲和丙都是不溶于水的白色固体物质,既能溶于盐酸又能溶于氢氧化钠溶液。
则甲是________,丙是________(填化学式)。写出“乙 丙”转化的离子方程式:______________________________。
丙”转化的离子方程式:______________________________。
(2)若乙溶液中加入KSCN溶液,有红色出现,则甲是______,丙是________(填化学式)。写出“甲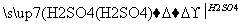 乙”转化的离子方程式:____________________________。
乙”转化的离子方程式:____________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
将6.85g Fe和Al的混合物溶于200mL 浓度为C mol/L的HNO3溶液中,得到标准状况下的NO、N2O混合气体共3.36L,测得反应后溶液的pH为0,再向所得溶液中加入过量NaOH溶液充分反应后生成沉淀质量为5.35 g。若不考虑反应前后溶液体积变化,则下列有关判断正确的是( )。
A.Fe与Al 的物质的量之比为1:1
B.混合气体中NO为0.03mol ,N2O为0.12mol
C.原HNO3溶液的浓度C=4 .9mol/L
.9mol/L
D.反应中被还原的HNO3为0.15mol
查看答案和解析>>
科目:高中化学 来源: 题型:
信息时代产生的大量电子垃圾对环境构成了极大的威胁。某“变废为宝”学生探究小组将一批废弃的线路板简单处理后,得到含70% Cu、25% Al、4% Fe及少量Au、Pt等金属的混合物,并设计出如下制备硫酸铜和 硫酸铝晶体的路线:
硫酸铝晶体的路线:
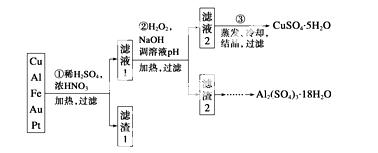
请回答下列问题:
(1)第①步Cu与酸反应的离子方程式为________________;得到滤渣1的主要成分为____________。
(2)第②步加H2O2的作用是______________,使用H2O2的优点是______________;调溶液pH的目的是使______________生成沉淀。
(3)用第③步所得CuSO4·5H2O制备无水CuSO4的方法是_______________________。
(4)由滤 渣2制取Al2(SO4)3·18H2O ,探究小组设计了三种方案:
渣2制取Al2(SO4)3·18H2O ,探究小组设计了三种方案:

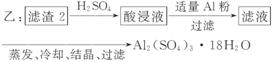
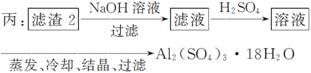
上述三种方案中,________方案不可行,原因是____________________________
_____________________________________________________________________;
从原子利用率角度考虑,__________方案更合理。
(5)探究小组用滴定法测定CuSO4·5H 2O (Mr=250)含量。取a g试样配成100 mL溶液,每次取20.00 mL,消除干扰离子后,用c mol·L-1 EDTA(H2Y2-)标准溶液滴定至终点,平均消耗EDTA溶液b mL。滴定反应如下:Cu2++H2Y2-===CuY2-+2H+
2O (Mr=250)含量。取a g试样配成100 mL溶液,每次取20.00 mL,消除干扰离子后,用c mol·L-1 EDTA(H2Y2-)标准溶液滴定至终点,平均消耗EDTA溶液b mL。滴定反应如下:Cu2++H2Y2-===CuY2-+2H+
写出计算CuSO4·5H2O质量分数的表达式w=______________________________;
下列操作会导致CuSO4·5H2O含量的测定结果偏高的是________。
a.未干燥锥形瓶
b.滴定终点时滴定管尖嘴中产生气泡
c.未除净可与EDTA反应的干扰离子
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是 ( )
A.因为SO2具有漂白性,所以它能使品红溶液、溴水、酸性高锰酸钾溶液、石蕊试液褪色
B.能使品红溶液褪色的不一定是SO2
C.SO2、漂白粉、活性炭、Na2O2都能使红墨水褪色,其原理相同
D.SO2和Cl2等物质的 量混合后通入装有湿润的有色布条的集气瓶中,漂白效果更好
量混合后通入装有湿润的有色布条的集气瓶中,漂白效果更好
查看答案和解析>>
科目:高中化学 来源: 题型:
2007年10月10日,德国科学家格哈德·埃尔特生日的当天获得了诺贝尔化学奖,以奖励他在表面化学领域做出的开拓性贡献。合成氨反应在铁催化剂表面进行时效率显著提高,就是埃尔特的研究成果。下列关于合成氨反应的叙述中,正确的是( )
A.铁作催化剂可加快反应速率,且有利于平衡向合成氨的方向移动
B.将氨从混合气中分离,可加快反应速率,且有利于平衡向合成氨的方向移动
C.升高温度可以加快反应速率,且有利于平衡向合成氨的方向移动
D.增大压强可加快反应速率,且有利于平衡向合成氨的方向移动
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com