
 25��ʱ���������ʵĵ��볣�������ʾ��
25��ʱ���������ʵĵ��볣�������ʾ��| ��ѧʽ | CH3COOH | H2CO3 | HClO |
| ���볣�� | 1.7��10-5 | K1=4.3��10-7 K2=5.6��10-11 | 3.0��10-8 |
���� ��1��������Ӷ�Ӧ�����ĵ���ƽ�ⳣ��Խ������������������Խ����
��2������������Դ���̼��������ӣ����߷�Ӧ����̼�����ƺʹ����
��3����pH��ͬʱ��Խ��ˮ����Σ���Ũ��Խ��
��4������Ϊ���ᣬϡ�����д���ĵ���̶�������Һ�������ӡ���������ӵ����ʵ�������������ʵ�����С��������Һ����仯�̶ȸ�������Һ�������ӡ���������ӡ������Ũ�ȼ�С������ˮ�����ӻ����䣬����Һ������������Ũ�����ݴ˽��н��
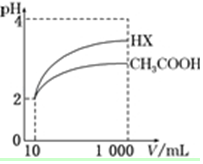
��5����ͼ��֪��ϡ����ͬ�ı�����HX��pH�仯�̶ȴ�������HXǿ������ƽ�ⳣ����ϡ�ͺ�HX�������ɵ�c��H+��С����ˮ�ĵ�����������С��
��� �⣺��1��������Ӷ�Ӧ�����ĵ���ƽ�ⳣ��Խ������������������Խ�������ڵ���ƽ�ⳣ��CH3COOH��H2CO3��HCO3-��HClO����ͬŨ��CH3COO-��HCO3-��CO32-��ClO-���H+��������ǿ������˳��Ϊ��CO32-��ClO-��HCO3-��CH3COO-��
�ʴ�Ϊ��c��d��b��a��
��2��NaClO��Һ��ͨ������CO2����Ӧ����̼�����ƺʹ����ᣬ��Ӧ�����ӷ���ʽΪ��ClO-+CO2+H2O=HCO3-+HClO���ʴ�Ϊ��ClO-+CO2+H2O=HCO3-+HClO����3��c��d��b��a
��3���������ʵ���Һ��a��Na2CO3��b��NaClO��c��CH3COONa��d��NaHCO3�����ӵ�ˮ��̶�˳���ǣ�b��a��d��c��pH��ͬ�������������ʵ���Һ�����ʵ���Ũ���ɴ�С��˳����b��a��d��c���ʴ�Ϊ��b��a��d��c��
��4��A��CH3COOH��Һ��ˮϡ�����У�������Һ�����������ĵ���̶Ƚ�С����ϡ�ͺ���Һ��c��H+����С����A��ȷ��
B��ϡ�����������ӵ����ʵ�������������ʵ�����С��������ͬһ��Һ�У���Һ�����ͬ�����ֵ����B����
C����Һ��c��H+��•c��OH-��֮��Ϊˮ�����ӻ���ϡ�ͺ���Һ�¶Ȳ��䣬��ˮ�����ӻ����䣬��C����
D��ϡ�����У�����ĵ���ƽ�ⳣ�����䣬����ѡ��ı�ֵ���䣬��D����
��ѡA��������Һ�����¶ȣ�������ʵĵ��������ȵģ������¶ȣ���ٽ����룬����������Ũ�����ӣ�ˮ���볣�����ӣ�����5�ֱ���ʽ�������������ABCD���ʴ�Ϊ��A��ABCD��
��5����ͼ��֪��ϡ����ͬ�ı�����HX��pH�仯�̶ȴ�������HXǿ������ƽ�ⳣ����ϡ�ͺ�HX�������ɵ�c��H+��С����ˮ�ĵ�����������С������HX��Һ��ˮ���������c��H+����
�ʴ�Ϊ�����ڣ����ڣ�
���� ���⿼����������ʵĵ���ƽ�⡢�ε�ˮ��ԭ�������ԵıȽϡ�pH�����ϡ�͵�֪ʶ����Ŀ�Ѷ��еȣ���ȷӰ�����ƽ�������Ϊ���ؼ���ע�������ϡ������������Ũ�ȼ�С������������Ũ������Ϊ�״��㣬����������ѧ�������Ӧ�û���֪ʶ��������


 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ������ʱ�ܶ�֮��Ϊ2��1 | |
| B�� | ԭ�������ʱ���еĵ�����֮��Ϊ1��4 | |
| C�� | �������ʱ���е�������֮��Ϊ4��5 | |
| D�� | ������ʱ���е�ԭ����֮��Ϊ1��2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 25�桢101kPaʱ��1mol������ȫȼ��ʱ���ų������������������ʵ�ȼ���� | |
| B�� | ��ʯȼ�����κ������¶��ܳ��ȼ�� | |
| C�� | ȼ���Ȼ��к����Ƿ�Ӧ�ȵ�����֮һ | |
| D�� | ����ͼ���кͷ�Ӧ����1molˮ����ʱ�ķ�Ӧ�Ƚ��к��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
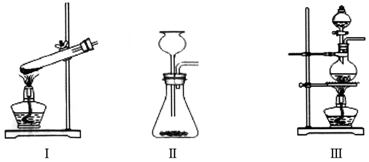
| A�� | 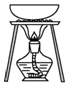 ���Ȼ�����Һ�еõ��Ȼ��ƾ��壬��ʹ����ͼ����ʾʵ��װ�� | |
| B�� |  ����ʯ�ͣ��õ����͡�ú�ͺͲ��͵ȸ�����֣���ʹ����ͼ����ʾʵ��װ�� | |
| C�� |  ʵ�����ư�����ʵ��װ����ͼ����ʾ | |
| D�� | 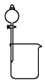 �����Ҵ�������Ļ��Һ��ʵ��װ����ͼ����ʾ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
 ��Fe2+��I-��Br-����Һ��ͨ���������������Һ���������ӵ����ʵ����仯��ͼ��ʾ����֪b-a=5���߶���ʾһ�ֺ����ᣬ�Ң�͢���ʾ�������к�����ͬ��Ԫ�أ�����˵������ȷ���ǣ�������
��Fe2+��I-��Br-����Һ��ͨ���������������Һ���������ӵ����ʵ����仯��ͼ��ʾ����֪b-a=5���߶���ʾһ�ֺ����ᣬ�Ң�͢���ʾ�������к�����ͬ��Ԫ�أ�����˵������ȷ���ǣ�������| A�� | �߶��ʾBr-�ı仯��� | B�� | ԭ��Һ��n��FeI2����n��FeBr2��=1��3 | ||
| C�� | �߶���ʾIO4-�ı仯��� | D�� | ����ͼ����Լ���a��ֵΪ6 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �þƾ���ȡ��ˮ�еĵ� | |
| B�� | �������к�ˮ���� | |
| C�� | �ù��˵ķ�����ȥNaCl��Һ�к��е��������۽��� | |
| D�� | �ü���-�����ķ������Գ�ȥ�����е�CaCl2��MgCl2������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com