
下列物质的稀溶液中,溶质的阴、阳离子个数之比为1:2的是( )
|
| A. | Na2HPO4 | B. | NaHSO4 | C. | (NH4)2SO4 | D. | K2S |
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
氧元素是地壳中含量最高的元素,请回答下列问题
(1)画出氧原子结构示意图 .
(2)元素周期表中氧元素的信息如图所示,从图中能直接获得的信息是 .
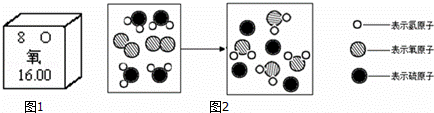
A.氧元素属于非金属元素
B.氧原子的核内的质子数为16
C.氧元素有O2和O3两种单质
(3)图2是硫化氢(H2S)在氧气中不完全燃烧反应的微观示意图.
写出该反应的化学方程式 ,该反应属于 (填基本反应类型)
查看答案和解析>>
科目:高中化学 来源: 题型:
室温下测得甲醛、乙醛和丙酮组成的液态混合物中氢元素的质量分数为9.8%,则该混合物的平均相对分子质量为()
A. 50 B. 49 C. 51 D. 44
查看答案和解析>>
科目:高中化学 来源: 题型:
向某溶液中缓缓通入Cl2至过量,此过程中一直未观察到有沉淀生成,该溶液中可能大量共存的离子组是()
A. CO32﹣、SO42﹣、K+、Na+ B. Ag+、NO3﹣、Cu2+、Na+
C. SO2、Ba2+、Cl﹣、K+ D. AlO2﹣、Br﹣、Na+、NO3﹣
查看答案和解析>>
科目:高中化学 来源: 题型:
Cr2O72﹣和CN﹣是工业废水中常见的污染物.若利用下列流程可对分别含两种离子的废水进行综合处理:
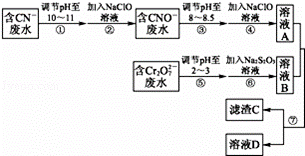
已知:Cr3+也有一定毒性,Cr3+在pH=6.0时开始沉淀,pH=8.0时沉淀完全.
回答下列问题:
(1)已知步骤②中无气体生成,写出反应的离子方程式: ,
步骤④中NaClO可将CNO﹣处理为完全无害的溶液,该过程中有两种无毒的不支持燃烧的气体产生,写出这两种气体的化学式: .
(2)步骤⑥的反应为S2O32﹣+Cr2O72﹣+H+﹣→SO42﹣+Cr3++H2O(未配平),则每处理1mol Cr2O72﹣转移6mol电子.
(3)滤渣C的化学式为Cr(OH)3,溶液A和溶液B混合可使废水中的Cr3+沉淀的原因是 .
(4)步骤⑦的操作名称为 ,若该操作在实验室中进行,则所需的玻璃仪器为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
对于反应N2+O2⇌2NO在密闭容器中进行,下列哪个条件不能加快化学反应速率( )
|
| A. | 缩小体积使压强增大 |
|
| B. | 体积不变充入N2使压强增大 |
|
| C. | 体积不变充入 He使压强增大 |
|
| D. | 升高温度 |
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)Zn粒和稀盐酸反应一段时间后,反应速率会减慢,当加热或加入浓盐酸后,反应速率明显加快.由此判断,影响化学反应速率的因素有 和 .
(2)元素周期表共有7周期,16族;同一周期元素的原子 相同.
(3)在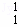 H、
H、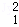 H、
H、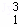 H、
H、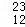 Mg、
Mg、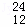 Mg和
Mg和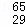 Cu中共有 种元素, 种原子.
Cu中共有 种元素, 种原子.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com